题目内容
已知温度T时水的离子积常数为KW。该温度下,将浓度为a mol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
| A.a = b |
| B.混合溶液的pH = 7 |
C.混合溶液中,c(H+) = 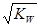 mol/L mol/L |
| D.混合溶液中,c(H+) + c(B-) = c(OH-) + c(A-) |
C
解析试题分析:只要溶液中c(H+) = c(OH-),则溶液就一定显中性,由于不能确定酸碱的强弱以及溶液的温度,所以选项AB不一定显中性。根据水的离子积常数可知,选项C中c(H+) = c(OH-),溶液显中性;D中符合电荷守恒,恒成立,不正确,答案选C。
考点:考查溶液酸碱性的判断。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将氨水缓缓地滴入盐酸中至中性,下列有关的说法:①盐酸过量 ②氨水过量 ③恰好完全反应 ④c (NH4+) = c(Cl-) ⑤c (NH4+) < c(Cl-) 正确的是
| A.②④ | B.③④ | C.②⑤ | D.①⑤ |
HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述中不正确的是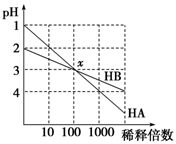
| A.HA是一种强酸 |
| B.x点,[A-]=[B-] |
| C.HB是一种弱酸 |
| D.原溶液中HA的物质的量浓度为HB的10倍 |
盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是
| A.在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO32-和OH- |
| B.NaHCO3溶液中:c(H+)+c(Na+)=c(HCO3-)+2c(CO32-)+c(OH-) |
| C.中和体积与物质的量浓度都相同的HCl溶液和CH3COOH溶液消耗NaOH物质的量相同 |
| D.中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗NaOH物质的量相同 |
用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,下列操作会引起测定结果偏高的是:(1)滴定时,装待测溶液的锥形瓶有少量水;(2)酸式滴定管用蒸馏水洗后,未用标准溶液洗;(3)滴定终点读数时,仰视刻度线 ( )
| A.只有(1) | B.只有(2) | C.(2)(3) | D.(1)(2)(3) |
25℃时,某溶液中由水电离产生的c(H+)和c(OH—)的乘积为1×10-20,下列说法正确的是
| A.该溶液的pH一定是10 | B.该溶液不可能pH=4 |
| C.该溶液的pH不可能是7 | D.不会有这样的溶液 |
已知NaHSO4在水中的电离方程式为:NaHSO4=Na++H++SO42-。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是
| A.该温度高于25℃ |
| B.由水电离出来的H+的浓度是1.0×10-12mol·L-1 |
| C.加入NaHSO4晶体抑制了水的电离 |
| D.该温度下加入等体积pH为12的NaOH溶液后溶液呈碱性 |
下列物质的水溶液,其中PH值小于7的是( )
| A.Na2CO3 | B.NH4NO3 | C.Na2SO4 | D.KNO3 |