题目内容
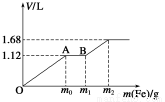
向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示。沉淀的生成与溶解的pH列于下表。以下推断正确的是( )
氢氧化物 | 溶液pH | |||
开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
Fe(OH)3 | 2.3 | 3.4 | - | - |
Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
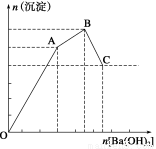
A.C点的沉淀为Fe(OH)3
B.OA段可能发生的反应有:3Ba2++6OH-+3SO42-+2Fe3+=3BaSO4↓+2Fe(OH)3↓
C.AB段可能发生的反应是:2SO42-+2Ba2++Al3++3OH-=2BaSO4↓+Al(OH)3↓
D.据图计算原溶液中c(Cl-)>c(SO42-)
B
【解析】发生的反应依次为
SO42-+Ba2+=BaSO4↓
Fe3++3OH-=Fe(OH)3↓
Al3++3OH-=Al(OH)3↓
Al(OH)3+OH-=AlO2-+2H2O
A项,C点应为BaSO4和Fe(OH)3沉淀,错误;B项正确;C项,AB段只发生生成Al(OH)3沉淀的反应,错误;D项,设一格代表1 mol,则n[Al(OH)3]=2 mol
n(BaSO4)=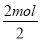 ×3=3 mol
×3=3 mol
所以n[Fe(OH)3]=6 mol-5 mol=1 mol
n(Cl-)=3 mol,所以c(Cl-)=c(SO42-),错误。

从下列事实所得出的相应结论正确的是( )
| 实验事实 | 结论 |
① | 在相同温度下,向1 mL 0.2 mol·L-1 NaOH溶液中滴入2滴0.1 mol·L-1 MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol·L-1 FeCl3溶液,又生成红褐色沉淀 | 溶解度:Mg(OH)2>Fe(OH)3 |
② | 将CO2通入到Na2SiO3溶液中产生白色浑浊 | 酸性:H2CO3>H2SiO3 |
③ | 已知反应5Cl2+I2+6H2O=2HIO3+10HCl,2BrO3-+Cl2=2ClO3-+Br2 | 氧化性强弱顺序:BrO3->Cl2>ClO3->IO3- |
④ | 测定等物质的量浓度的Na2SO4与Na2CO3溶液的pH,后者较大 | 非金属性:S>C |
A.③④ B.②④ C.①②③ D.全部