题目内容
向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式 。
(2)整个过程中的还原剂是 。
(3)把KI换成KBr,则CCl4层变为 色;继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是 。
(4)加碘盐中含碘量为20~50 mg·kg-1。制取加碘盐(含KIO3的食盐)1 000 kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2 L(标准状况,保留2位小数)。
(1)I2+5Cl2+6H2O=2HIO3+10HCl
(2)KI、I2 (3)红棕 HBrO3>Cl2>HIO3 (4)10.58
【解析】(1)CCl4层变成紫色说明有I2生成,继续滴加氯水变成无色,说明I2又被氧化生成HIO3,同时生成HCl。(2)首先KI被氧化生成I2,后来I2又被氧化生成KIO3,所以整个过程中的还原剂是KI、I2。(3)Br2的CCl4溶液显红棕色;继续滴加氯水,CCl4层颜色没有变化,说明氯水能氧化I2但不能氧化Br2,结合第(1)问可得氧化性HBrO3>Cl2>HIO3。(4)KI被Cl2氧化成KIO3,对应关系式为
I- ~ KIO3 ~ 3Cl2
1 mol 3 mol
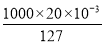 mol n(Cl2)
mol n(Cl2)
则n(Cl2)=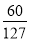 mol,V(Cl2)=
mol,V(Cl2)=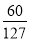 mol×22.4 L·mol-1≈10.58 L。
mol×22.4 L·mol-1≈10.58 L。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示。沉淀的生成与溶解的pH列于下表。以下推断正确的是( )
氢氧化物 | 溶液pH | |||
开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
Fe(OH)3 | 2.3 | 3.4 | - | - |
Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
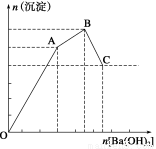
A.C点的沉淀为Fe(OH)3
B.OA段可能发生的反应有:3Ba2++6OH-+3SO42-+2Fe3+=3BaSO4↓+2Fe(OH)3↓
C.AB段可能发生的反应是:2SO42-+2Ba2++Al3++3OH-=2BaSO4↓+Al(OH)3↓
D.据图计算原溶液中c(Cl-)>c(SO42-)
