题目内容
A、B、C、D四种短周期元素,它们的原子序数依次增大,其中A与C及B与D分别是同主族元素;已知B、D两元素间可形成DB2和DB3两种化合物,两者相对分子质量相差16;又知A、C两元素原子序数之和是B、D两元素原子序数之和的(1)写出由A、B、C三元素形成的化合物的电子式___________,其晶体中所含化学键的类型有___________。
(2)A2B与A2D的沸点:A2B___________A2D(填“高于”或“低于”),其原因是___________________________________。
(3)由A、B、C、D四种元素形成的物质X,与盐酸反应能够生成具有刺激性气味的气体,写出X与盐酸反应的离子方程式_____________________________________________________。
![]() 离子键、共价键
离子键、共价键
(2)高于 H2O分子之间能形成氢键
(3)![]() +H+
+H+![]() SO2↑+H2O
SO2↑+H2O
解析:已知B、D两元素间可形成DB2和DB3两种化合物,两者相对分子质量相差16,则推出B的相对原子质量为16,所以B为O;又因为B、D同主族,且D的原子序数大于B,所以D为S;B、D原子序数之和的![]() 是12,又因A、C同主族,所以A为H;C为Na。
是12,又因A、C同主族,所以A为H;C为Na。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
A、B、C、D四种短周期元素的原子半径依次减小,A与C的核电荷数之比3:4,D分别与A、B、C可形成10个电子的分子X、Y、Z.则下列叙述正确的是( )
| A、X、Y、Z三种分子的稳定性逐渐减弱 | B、上述四种元素共能形成五种单质 | C、X、Y、Z三种分子的沸点逐渐升高 | D、X、Y、Z三种分子均为极性分子 |

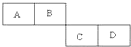 A、B、C、D四种短周期元素在周期表中的相对位置如表所示,A的单质与水蒸气反应可以制取水煤气.
A、B、C、D四种短周期元素在周期表中的相对位置如表所示,A的单质与水蒸气反应可以制取水煤气.