题目内容
15.下列性质适合分子晶体的是( )| A. | 能溶于CS2,熔点112.8℃,沸点444.6℃ | |
| B. | 熔点1003.1℃,液态时导电,水溶液导电 | |
| C. | 熔点1070℃,易溶于水,水溶液能导电 | |
| D. | 熔点97.81℃,质软,导电,密度0.97 g•cm-3 |
分析 分子晶体是由分子构成,分子间的作用力很弱,具有较低的熔点、沸点、硬度小、易挥发等性质.
解答 解:A.单质硫能溶于CS2、熔点112.8℃,沸点444.6℃,单质硫是分子晶体,故A正确;
B.熔点为1003.1℃,熔点高,不符合分子晶体的特点,液态时导电,是由于液态时,存在离子,符合离子晶体特点,故B错误;
C.分子晶体是由分子构成,许多物质在常温下呈气态或液态,其溶解性遵守“相似相溶”原理,熔点1070℃,与分子晶体的特点严重不符,易溶于水,水溶液导电,有的分子晶体具有此特点,如氯化氢晶体就具有,故C错误;
D.金属钠熔点为97.81℃,质软、导电、密度0.97g/cm3,金属钠为金属晶体,故D错误,故选A.
点评 本题主要考查了分子晶体的物理性质,解题时需掌握分子晶体熔沸点等显著物理性质即可解答,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.下列叙述正确的是( )
| A. | 在同温同压下,甲容器中的氧气(O2)和乙容器中的氨气(NH3)所含的原子个数相同,则甲、乙两容器中气体的体积之比为1:2 | |
| B. | 任何条件下,等物质的量的甲烷(CH4)和一氧化碳所含的原子数一定相等 | |
| C. | 在标准状况时,20ml NH3与60ml N2所含的原子个数比为1:3 | |
| D. | 同温同压下,1L一氧化碳气体一定比1L氧气的质量小 |
3.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 2 mol•L-1 的Na2SO4溶液中含有4NA个Na+ | |
| B. | 16克甲烷所含的电子数为10NA | |
| C. | 常温常压下,11.2L氧气中所含有的原子数为NA | |
| D. | NA个水分子的相对分子质量之和等于水的摩尔质量 |
10.室温下,向a mol/L氨水中逐滴加入等浓度的盐酸,至完全中和,下列描述不正确的是( )
| A. | pH逐渐减小 | B. | n(NH4+)增大 | ||
| C. | 恰好中和时水溶液显中性 | D. | Kw不变 |
12.有机化合物中必须含有的元素是( )
| A. | 氢 | B. | 氮 | C. | 氧 | D. | 碳 |
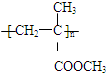 它的链节为
它的链节为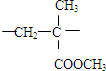 ,设其平均聚合度为3000,则该高聚物得平均相对分子质量为300 000.从结构角度看它应该属于线 型高分子.试推测有机玻璃能溶于CHCl3,具有热塑(填“热塑”或“固热”)性.
,设其平均聚合度为3000,则该高聚物得平均相对分子质量为300 000.从结构角度看它应该属于线 型高分子.试推测有机玻璃能溶于CHCl3,具有热塑(填“热塑”或“固热”)性. 在如图所示装置中,试管A、B中的电极为多孔的惰性电极;C、D为两个铂夹夹在被Na2SO4溶液浸湿的滤纸条上,滤纸条的中部滴有KMnO4液滴;电源有a、b两极.若在A、B中充满KOH溶液后倒立于盛KOH溶液的水槽中,断开K1,闭合K2、K3,通直流电,实验现象如图所示,请回答下列问题
在如图所示装置中,试管A、B中的电极为多孔的惰性电极;C、D为两个铂夹夹在被Na2SO4溶液浸湿的滤纸条上,滤纸条的中部滴有KMnO4液滴;电源有a、b两极.若在A、B中充满KOH溶液后倒立于盛KOH溶液的水槽中,断开K1,闭合K2、K3,通直流电,实验现象如图所示,请回答下列问题