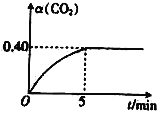
题目内容
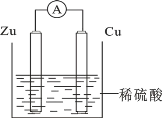
【题目】如图所示甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:
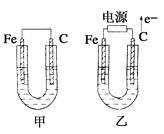
(1)若两池中电解质溶液均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的________棒,乙池中的________棒。
②甲池中负极的电极反应式是____________________________________________。
(2)若两池中电解质溶液均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式:______________________________________________。
②乙池碳棒上电极反应属于________(填“氧化反应”或“还原反应”)。
【答案】碳 铁 Fe-2e- =Fe2+ 2Cl-+2H2O![]() Cl2↑+H2↑+2OH- 氧化反应
Cl2↑+H2↑+2OH- 氧化反应
【解析】
(1)甲池为原电池,铁做负极,碳棒作正极,依据氧化还原反应的规律和原电池的工作原理作答;
(2)若电解质溶液为饱和氯化钠溶液,则依据电子的流动方向判断出Fe为阴极,C棒为阳极,再结合电解池的工作原理作答。
(1)①甲池为原电池,原电池中活泼金属做负极,发生氧化反应,碳棒做正极,有红色的Cu析出,乙池为电解池,外电路电子流向电源正极,所以碳棒为阳极,放出氯气,阴极铁电极上发生还原反应有红色的Cu单质析出,故答案为:碳;铁;
②甲池中负极铁失电子生成Fe2+,其电极反应式为Fe-2e-=Fe2+;
(2)①若电解质溶液为饱和氯化钠溶液,则乙池为用惰性电极为阳极电解氯化钠溶液,方程式为:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-;
Cl2↑+H2↑+2OH-;
②乙池碳棒为电解池的阳极,发生的是失电子的氧化反应,故答案为:氧化反应。

【题目】(本题共8分)现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第三周期元素的简单离子中半径最小 |
(1)写出元素T的原子结构示意图 。
(2)元素Y与元素Z相比,金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________(填序号)。
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈
d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式:_____ _________。
(4)元素T和氢元素可形成一种18电子的化合物Q,元素X与氢元素也能按原子个数比为1∶2形成一种18电子化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式: 。