题目内容
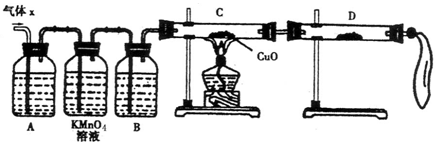
(本题共16分)防治环境污染是当前环保工作的重要研究内容之一。二氧化硫和氮氧化物是大气的主要污染物。
1.将1.5 mol SO2用氢氧化钠溶液、石灰及氧气处理后,假设硫元素不损失,理论上可得到_________________g石膏(CaSO4?2H2O)。
2.用CH4消除NOx污染的化学方程式为:
CH4+4NO → 2N2+CO2+2H2O; CH4+2NO2 → N2+CO2+2H2O
现有11.2 L NO2、NO的混合气体NOx,将其还原为N2,需要4.48 L 的CH4,则混合气体中NO2、NO的物质的量分别为___________________。(体积都已换算为标准状况)
3.(1)常温下用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2,同时ZnFe2Oy转变为ZnFe2O4。若2 mol ZnFe2Oy与足量NO2可生成0.5 mol N2,则y=_______________。
(2)氧缺位铁酸锌ZnFe2Oz化学式的氧化物形式为aZnO?bFeO?cFe2O3。已知1 mol ZnFe2Oz最多能使4.0 L(标况)NO1.4转化为N2。则上述氧化物形式的化学式可具体表示为______________________________。
4.低温臭氧氧化脱硫脱硝技术可以同时吸收烟气中的氮氧化物和二氧化硫,反应原理是将NOx氧化成N2O5,通过洗涤形成硝酸盐,二氧化硫形成硫酸盐。其主要反应如下:
NO+O3 → NO2+O2 ……………………………………………①
2NO2+O3 → N2O5+O2 …………………………………………②
N2O5+2NH3+H2O → 2NH4NO3 ………………………………③
SO2+O3+2NH3+H2O → (NH4)2SO4+O2 ……………………④
某热电厂烟气中平均含NOx 4.5‰、SO2 9.0‰(体积分数),压缩空气经臭氧发生器变成臭氧空气,其中O3浓度为90 L/m3,臭氧空气与加湿氨气和烟气混合反应。若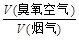 流量比为y,请通过计算列出y与x的关系式。
流量比为y,请通过计算列出y与x的关系式。
1.将1.5 mol SO2用氢氧化钠溶液、石灰及氧气处理后,假设硫元素不损失,理论上可得到_________________g石膏(CaSO4?2H2O)。
2.用CH4消除NOx污染的化学方程式为:
CH4+4NO → 2N2+CO2+2H2O; CH4+2NO2 → N2+CO2+2H2O
现有11.2 L NO2、NO的混合气体NOx,将其还原为N2,需要4.48 L 的CH4,则混合气体中NO2、NO的物质的量分别为___________________。(体积都已换算为标准状况)
3.(1)常温下用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2,同时ZnFe2Oy转变为ZnFe2O4。若2 mol ZnFe2Oy与足量NO2可生成0.5 mol N2,则y=_______________。
(2)氧缺位铁酸锌ZnFe2Oz化学式的氧化物形式为aZnO?bFeO?cFe2O3。已知1 mol ZnFe2Oz最多能使4.0 L(标况)NO1.4转化为N2。则上述氧化物形式的化学式可具体表示为______________________________。
4.低温臭氧氧化脱硫脱硝技术可以同时吸收烟气中的氮氧化物和二氧化硫,反应原理是将NOx氧化成N2O5,通过洗涤形成硝酸盐,二氧化硫形成硫酸盐。其主要反应如下:
NO+O3 → NO2+O2 ……………………………………………①
2NO2+O3 → N2O5+O2 …………………………………………②
N2O5+2NH3+H2O → 2NH4NO3 ………………………………③
SO2+O3+2NH3+H2O → (NH4)2SO4+O2 ……………………④
某热电厂烟气中平均含NOx 4.5‰、SO2 9.0‰(体积分数),压缩空气经臭氧发生器变成臭氧空气,其中O3浓度为90 L/m3,臭氧空气与加湿氨气和烟气混合反应。若
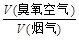 流量比为y,请通过计算列出y与x的关系式。
流量比为y,请通过计算列出y与x的关系式。(本题共16分)
1. 258(2分)
2. 0.3 mol 、0.2 mol(4分)。
3.(1)3(3分)。(2)4ZnO?2FeO?3Fe2O3(3分)。
4.(4分)由反应①②可知,O3在氧化过程中都生成O2,则NOx与O3反应时有如下关系:
2NOx + (5-2x)O3 + H2O → 2HNO3 + (5-2x)O2
设烟气为1m3,其中NOx为4.5L,SO2为9L,则有
2NOx ~ (5-2x)O3
2 5-2x
4.5 90y-9
解之y=0.225-0.05x
1. 258(2分)
2. 0.3 mol 、0.2 mol(4分)。
3.(1)3(3分)。(2)4ZnO?2FeO?3Fe2O3(3分)。
4.(4分)由反应①②可知,O3在氧化过程中都生成O2,则NOx与O3反应时有如下关系:
2NOx + (5-2x)O3 + H2O → 2HNO3 + (5-2x)O2
设烟气为1m3,其中NOx为4.5L,SO2为9L,则有
2NOx ~ (5-2x)O3
2 5-2x
4.5 90y-9
解之y=0.225-0.05x
1.由S的守恒: SO2 ~ CaSO4?2H2O
2.由题意得:2CH4 + 5NOx→5/2N2 + 2CO2 +4H2O ,由O原子守恒可知x=8/5
再由十字交叉法可知:NO为0.2mol 、NO2为0.3mol
3.(1)由题意及原子守恒可知:2 ZnFe2Oy+ 1 NO2→0.5 mol N2 + 2ZnFe2O4,
由氧原子守恒:2y+2=2×4,知y=3
(2)1 ZnFe2Oz+ 1/4 NO1.4→ 1/8 mol N2 + 1ZnFe2O4可求出,z=15/4
则 ZnFe2O15/4可写作 Zn4Fe8O15,可拆解为4ZnO?2FeO?3Fe2O3
2.由题意得:2CH4 + 5NOx→5/2N2 + 2CO2 +4H2O ,由O原子守恒可知x=8/5
再由十字交叉法可知:NO为0.2mol 、NO2为0.3mol
3.(1)由题意及原子守恒可知:2 ZnFe2Oy+ 1 NO2→0.5 mol N2 + 2ZnFe2O4,
由氧原子守恒:2y+2=2×4,知y=3
(2)1 ZnFe2Oz+ 1/4 NO1.4→ 1/8 mol N2 + 1ZnFe2O4可求出,z=15/4
则 ZnFe2O15/4可写作 Zn4Fe8O15,可拆解为4ZnO?2FeO?3Fe2O3

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目