题目内容
【题目】燃烧法是测定有机化合物化学式的一种重要方法。在一定温度下取0.1 mol某气态烃A在O2中完全燃烧,生成CO2和水蒸汽,放出热量QkJ,将生成物依次通过浓硫酸和碱石灰,浓硫酸增重7.2 g,碱石灰增重17.6 g。将烃A加入酸性KMnO4溶液或Br2的CCl4溶液,均能使它们褪色。
(1)写出烃A的分子式 ;
(2) 已知烃A分子结构高度对称且有两个甲基,请写出烃A的结构简式 ;
(3)写出烃A使Br2的CCl4溶液褪色的化学方程式 ;
(4)烃A在一定条件下可以通过加聚反应合成一种塑料,则该反应的化学方程式是 。
【答案】(1)C4H8;(2)CH3CH=CHCH3;(3)CH3CH=CHCH3+Br2 → CH3CHBrCHBrCH3;
(4)nCH3CH=CHCH3→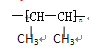
【解析】

![]()
![]() 试题分析:(1)浓硫酸增重为水的质量,为7.2克,即7.2/18=0.4摩尔,碱石灰增重为17.6克,即17.6/44=0.4摩尔则,有机物中含有的碳原子数为0.4/0.1=4,氢原子数为0.4×2/0.4=8,则分子式为C4H8;(2)因为A有两个甲基,且对称,所以结构为CH3CH=CHCH3; (3)2-丁烯与溴的四氯化碳发生加成反应生成2,3-二溴丁烷,方程式为:CH3CH=CHCH3+Br2 → CH3CHBrCHBrCH3;(4)2-丁烯在一定条件下发生加聚反应生成聚2-丁烯,方程式为:nCH3CH=CHCH3 →
试题分析:(1)浓硫酸增重为水的质量,为7.2克,即7.2/18=0.4摩尔,碱石灰增重为17.6克,即17.6/44=0.4摩尔则,有机物中含有的碳原子数为0.4/0.1=4,氢原子数为0.4×2/0.4=8,则分子式为C4H8;(2)因为A有两个甲基,且对称,所以结构为CH3CH=CHCH3; (3)2-丁烯与溴的四氯化碳发生加成反应生成2,3-二溴丁烷,方程式为:CH3CH=CHCH3+Br2 → CH3CHBrCHBrCH3;(4)2-丁烯在一定条件下发生加聚反应生成聚2-丁烯,方程式为:nCH3CH=CHCH3 →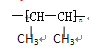 。
。

【题目】IA、B、C、D四种元素的核电荷数均小于18,A元素原子核外只有1个电子;B是地壳中含量最多的元素;B、C可形成两种化合物CB和CB2,C的最高正价与最低负价绝对值相等,CB有毒,CB2可用于灭火;D+具有与Ne原子相同的电子层结构。

(1)试判断A、B、C、D四种元素的名称。A______,B_____,C______,D______。
(2)C在周期表中的位置是 。
(3)由B、D两种元素组成的D2B2型化合物的电子式为_______,CB2的电子式 为________。
(4)如右图所示,在烧瓶中收集满CB2气体,用带导管(导管一端事先绑好一个气球)的胶塞紧,当打开胶塞迅速倒入浓的A、B、D三种元素组成的化合物的溶液后,立即塞紧胶塞振荡,可观察到_____,原因是_____________。
II(9分)下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:
主族K] | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | [m] | ⑩ |
(1)在最高价氧化物的水化物中,酸性最强的化合物的分子式是: ,碱性最强的化合物的电子式是: 。
(2)最高价氧化物是两性氧化物的元素是 ;写出它的氧化物与氢氧化钠反应的离子方程式 。
(3)用电子式表示元素④与⑥的化合物的形成过程:
(4)表示①与⑦的化合物的电子式 ,该化合物是由 (填“极性”“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是______(要求用离子符号表示)。
(6)元素③的氢化物常温下和元素⑦的单质反应的离子方程式为: 。