题目内容
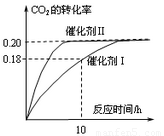
已知CO2可以生产绿色燃料甲醇.CO2(g)+3H2(G)![]() CH3OH(g)+H2O(g);ΔH=-187.4 kJ·mol-1.300℃时.密闭容器中,当C(CO2)=1.00 mol·L-1C(H2)=1.60 mol·L-1开始反应,结果如下图所示,回答下列问题:
CH3OH(g)+H2O(g);ΔH=-187.4 kJ·mol-1.300℃时.密闭容器中,当C(CO2)=1.00 mol·L-1C(H2)=1.60 mol·L-1开始反应,结果如下图所示,回答下列问题:
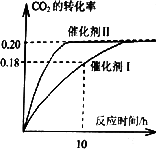
(1)使用催化剂Ⅰ时,反应在10小时内的平均反应速率:V(H2)=________mol·(L·h)-1.
(2)下列叙述正确的是________.
A
.容器内气体的密度不再改变时,反应不一定达到平衡状态B.充人氩气増大压强有利于提髙CO2的转化率
C
.CO2平衡转化率:在上述反应条件下,催化剂Ⅱ比催化剂Ⅰ高D
.催化效率:在上述反应条件下,催化剂Ⅱ比催化剂Ⅰ高(3)将上述平衡体系升温至400℃,平衡常数:K(400℃)________K(300℃)(填<、=或>).
(4)已知:2H2(g)+O2(g)=2H2O(g);ΔH=-242.8 kJ·mol-1则反应2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g);ΔH=________kJ·mol-1.
答案:

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
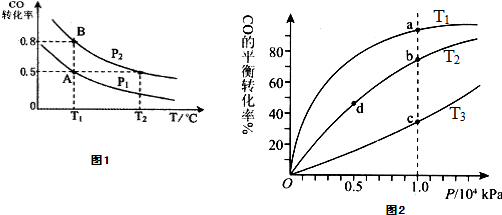
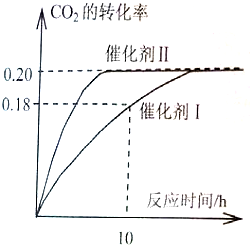 已知CO2可以生产绿色燃料甲醇.
已知CO2可以生产绿色燃料甲醇. CH3OH(g) + H2O(g) ΔH=-187.4 kJ/mol。3000C时的恒容密闭容器中,当C(CO2) = 1.00 mol.L-1 C(H2) =" 1.60" mol.L-1开始反应,结果如右图所示,回答下列问题:
CH3OH(g) + H2O(g) ΔH=-187.4 kJ/mol。3000C时的恒容密闭容器中,当C(CO2) = 1.00 mol.L-1 C(H2) =" 1.60" mol.L-1开始反应,结果如右图所示,回答下列问题: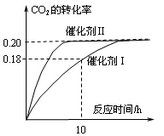
 CH3OH(g) + H2O(g)
ΔH=-187.4 kJ/mol。3000C时的恒容密闭容器中,当C(CO2) = 1.00 mol.L-1 C(H2)
=" 1.60" mol.L-1开始反应,结果如右图所示,回答下列问题:
CH3OH(g) + H2O(g)
ΔH=-187.4 kJ/mol。3000C时的恒容密闭容器中,当C(CO2) = 1.00 mol.L-1 C(H2)
=" 1.60" mol.L-1开始反应,结果如右图所示,回答下列问题: