题目内容
2.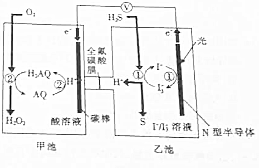 我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2─H2O2+S↓.
我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2─H2O2+S↓.已知甲池中发生的反应为:
 下列说法正确的是( )
下列说法正确的是( )| A. | 该装置将电能转化为光能 | |
| B. | H+从甲池移向乙池 | |
| C. | 甲池中碳棒上发生的电极反应为AQ+2H+-2e-=H2AQ | |
| D. | 乙池溶液中发生的反应为H2S+I3-═3I-+S↓+2H+ |
分析 A、装置是原电池装置,据此确定能量变化情况;
B、原电池中阳离子移向正极;
C、甲池中碳棒是正极,该电极上发生得电子的还原反应;
D、在乙池中,硫化氢失电子生成硫单质,碘单质得电子生成I-,据物质的变化确定发生的反应.
解答 解:A、装置的是原电池装置,根据图中信息知道是将光能转化为电能的装置,故A错误;
B、原电池中阳离子移向正极,甲池中碳棒是正极,所以氢离子从乙池移向甲池,故B错误;
C、甲池中碳棒是正极,该电极上发生得电子的还原反应,即AQ+2H++2e-=H2AQ,故C错误;
D、在乙池中,硫化氢失电子生成硫单质,碘单质得电子生成I-,发生的反应为H2S+I3-═3I-+S↓+2H+,故D正确.
故选D.
点评 本题考查学生原电池的工作原理以及电极反应式的书写知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目
10.常温下,PH都等于5的盐酸、醋酸、氯化铵溶液中,水的电离度分别为a1、a2、a3,则他们的关系是( )
| A. | a1=a2>a3 | B. | a1>a2>a3 | C. | a1=a2<a3 | D. | a1<a2<a3 |
17.下列选项中,有关实验操作、现象和结论都正确的是( )
| 实验操作 | 现象 | 结论 | |
| A | 将过量的CO2通入CaCl2溶液中 | 无白色沉淀出现 | 生成的Ca(HCO3)2可溶于水 |
| B | 常温下将Al片插入浓硫酸中 | 无明显现象 | Al片和浓硫酸不反应 |
| C | 将铜片放入过量的稀硝酸中 | 生成无色气体,后观察到红棕色 | NO遇氧气反应生成红棕色的NO2 |
| D | 将SO2通入溴水中 | 溶液褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
7.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 4.48 L H2和O2的混合气体中所含分子数为0.2NA | |
| B. | 标准状况下,1.8g的H2O中含有的电子数为0.1NA | |
| C. | 53.5 g氯化铵晶体中含有NH4+的数目为NA | |
| D. | 标准状况下,22.4 L氦气所含有的原子数为2NA |
11.设NA为阿伏加德罗常数,下列说法不正确的是( )
| A. | 标准状况下22.4L的四氯化碳,含有四氯化碳分子数为NA | |
| B. | 23g金属钠变为钠离子时失去的电子数为NA | |
| C. | 2.0g重水(D2O)中含有的中子数为NA | |
| D. | 常温常压下,48gO3和O2混合气体中含有的氧原子数为3NA |
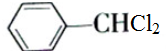 ,沸点206℃)是合成苯甲醛的中间体,实验室合成苄叉二氯的装置如图所示.
,沸点206℃)是合成苯甲醛的中间体,实验室合成苄叉二氯的装置如图所示.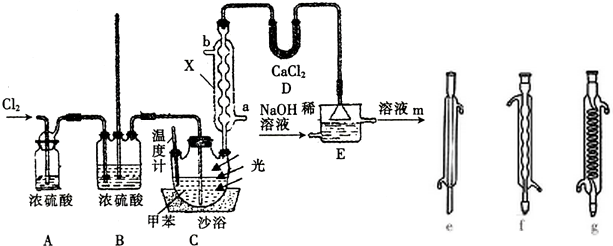
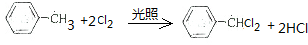 .
.