题目内容
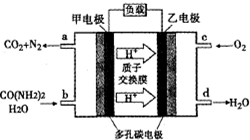 化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于描述正确的是( )
化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于描述正确的是( )| A、电池工作时H+移向负极 |
| B、该电池用的电解质溶液是KOH溶液 |
| C、甲电极反应式为:CO(NH2)2+H2O-6e-═CO2+N2+6H+ |
| D、电池工作时,理论每有净化1mol CO(NH2)2,消耗33.6L O2 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、原电池中阳离子向正极移动;
B.该原电池是酸性电解质;
C.负极上是CO(NH2)2失电子生成二氧化碳和氮气;
D.根据电池的总反应式进行计算.
B.该原电池是酸性电解质;
C.负极上是CO(NH2)2失电子生成二氧化碳和氮气;
D.根据电池的总反应式进行计算.
解答:
解:A、原电池中阳离子向正极移动,则电池工作时H+移向正极,故A错误;
B.该原电池是酸性电解质,质子交换膜只允许氢离子通过,故B错误;
C.负极上是CO(NH2)2失电子生成二氧化碳和氮气,则负极反应式为:CO(NH2)2+H2O-6e-=CO2+N2+6H+,故C正确;
D.电池的总反应式为:2CO(NH2)2+3O2=2CO2+2N2+4H2O,每净化1mol CO(NH2)2,消耗1.5molO2,则在标准状况下氧气为33.6L,由于没说明是标准状况,所以氧气的体积不能求算,故D错误;
故选C.
B.该原电池是酸性电解质,质子交换膜只允许氢离子通过,故B错误;
C.负极上是CO(NH2)2失电子生成二氧化碳和氮气,则负极反应式为:CO(NH2)2+H2O-6e-=CO2+N2+6H+,故C正确;
D.电池的总反应式为:2CO(NH2)2+3O2=2CO2+2N2+4H2O,每净化1mol CO(NH2)2,消耗1.5molO2,则在标准状况下氧气为33.6L,由于没说明是标准状况,所以氧气的体积不能求算,故D错误;
故选C.
点评:本题考查了原电池原理的应用,注意掌握电极方程式的书写是解决本题的关键,注意用气体的体积求算物质的量是要看清是否是标准状况,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列无色透明溶液,能大量共存的是( )
| A、K+、Na+、HCO3-、OH- |
| B、Cl-、MnO4-、K+、Na+ |
| C、SO42-、K+、Cl-、NO3- |
| D、H+、NO3-、CO32-、Fe2+ |
下列有机物中,不属于烃的衍生物的是( )
| A、卤代烃 | B、酒精 |
| C、氯仿 | D、邻甲基乙苯 |
下列反应属于置换反应的是( )
| A、CaO+CO2═CaCO3 |
| B、NaCl+AgNO3═AgCl↓+NaNO3 |
| C、NH4Cl═NH3↑+HCl↑ |
| D、Mg+2HCl═MgCl2+H2↑ |
0.3mol Cu与足量的稀HNO3完全反应时,被还原的HNO3的物质的量是( )
| A、0.3mol |
| B、0.6mol |
| C、0.4mol |
| D、0.2mol |
某有机物的结构简式为CH2=CH-CH2-CH2OH,下列关于该有机物的叙述不正确的是( )
| A、能与金属钠发生反应并放出氢气 |
| B、能在催化剂作用下与H2发生加成反应 |
| C、属于烃类物质 |
| D、在浓H2SO4催化下能与乙酸发生酯化反应 |
化学与人类生活、社会可持续发展密切相关.下列说法不正确的是( )
| A、如将某材料分散到液体分散剂中,该分散系可发生丁达尔效应,由此可推测该材料粒子的直径为1~100nm之间 |
| B、质谱法是测定有机物组成和结构的现代分析方法之一,同位素示踪法是科学家经常使用的研究化学反应历程的手段之一 |
| C、发酵粉中含有苏打,能使焙制出的糕点疏松多孔 |
| D、高空臭氧层吸收太阳紫外线,保护地球生物;低空臭氧是污染气体,对人体有危害 |
下列物质含有离子键的是( )
| A、N02 |
| B、H20 |
| C、HCl |
| D、KCl |
针对实验室制取氨气,下列说法不正确的是( )
| A、发生装置与用KClO3制取O2的装置相同 |
| B、可用排饱和氯化铵溶液的方法收集氨气 |
| C、氨气的验满可以用湿润的红色石蕊试纸或沾有浓盐酸的玻璃棒放于试管口附近 |
| D、所用的铵盐不是NH4NO3,是因为NH4NO3受热易爆炸 |