题目内容
0.3mol Cu与足量的稀HNO3完全反应时,被还原的HNO3的物质的量是( )
| A、0.3mol |
| B、0.6mol |
| C、0.4mol |
| D、0.2mol |
考点:化学方程式的有关计算
专题:计算题
分析:被还原的硝酸生产NO,根据电子转移守恒计算被还原的硝酸.
解答:
解:被还原的硝酸生产NO,根据电子转移守恒,被还原的硝酸物质的量=
=0.2mol,故选D.
| 0.3mol×2 |
| 5-2 |
点评:本题考查化学方程式有关计算,比较基础,注意利用电子转移守恒.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
下列叙述正确的是( )
| A、Al、Fe、Cu在潮湿空气中放置一段时间后均只生成氧化物 |
| B、金属Mg与稀硫酸和CO2均能反应,其反应类型相同 |
| C、浓盐酸和浓硫酸暴露在空气中浓度都会降低,其原因相同 |
| D、氯气具有很强的氧化性,在化学反应中只能做氧化剂 |
冶金工业上常用电解熔融MgCl2而不用电解MgO的方法制取镁,其原因是( )
| A、熔融的MgO不导电 |
| B、MgO分子间作用力很大 |
| C、MgO熔点高 |
| D、MgO属原子晶体 |
下列物质在水中最难电离的是( )
| A、CH3COOH |
| B、CH3CH2OH |
| C、H2CO3 |
D、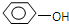 |
在盐类发生水解的过程中,下列说法正确的是( )
| A、盐的水解不属于离子反应 |
| B、溶液的pH发生改变 |
| C、水的电离程度逐渐增大 |
| D、没有中和反应发生 |
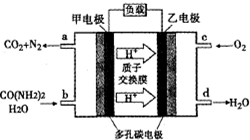 化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于描述正确的是( )
化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于描述正确的是( )| A、电池工作时H+移向负极 |
| B、该电池用的电解质溶液是KOH溶液 |
| C、甲电极反应式为:CO(NH2)2+H2O-6e-═CO2+N2+6H+ |
| D、电池工作时,理论每有净化1mol CO(NH2)2,消耗33.6L O2 |
在温度不变,恒容的容器中进行反应2HI?H2+I2(正反应为吸热反应),反应物的浓度由1mol?L-1降到0.6mol?L-1需2s,那么由0.6mol?L-1降到0.2mol?L-1所需的时间为( )
| A、等于1s | B、等于2s |
| C、大于2s | D、下于2s |
下列物质分类不正确的是( )
| A、氧化铜属于氧化物 |
| B、淀粉属于天然高分子化合物 |
| C、纯碱属于碱类 |
| D、漂白粉属于混合物 |
下列物质无法通过单质与O2直接化合生成的是( )
| A、Na2O2 |
| B、Al2O3 |
| C、SO3 |
| D、NO |