题目内容
下列物质含有离子键的是( )
| A、N02 |
| B、H20 |
| C、HCl |
| D、KCl |
考点:离子键的形成
专题:化学键与晶体结构
分析:一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,第IA、第IIA族和第VIA、第VIIA族元素之间易形成离子键,离子化合物中一定含有离子键.
解答:
解:A.N02中只存在N、O形成的共价键,故A错误;
B.H20中只存在H、O形成的共价键,故B错误;
C.HCl中只存在H、Cl形成的共价键,故C错误;
D.KCl中只含钾离子与氯离子形成的离子键,故D正确;
故选D.
B.H20中只存在H、O形成的共价键,故B错误;
C.HCl中只存在H、Cl形成的共价键,故C错误;
D.KCl中只含钾离子与氯离子形成的离子键,故D正确;
故选D.
点评:本题考查化学键,把握化学键形成的一般规律为解答的关键,注意特殊物质中的化学键(如氯化铝、铵盐)即可解答,题目难度不大.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
下列叙述不正确的是( )
| A、NH3易液化,液氨常用作制冷剂 |
| B、浓HNO3 的氧化性强于稀HNO3 |
| C、氨盐受热易分解,因此贮存氨态氮肥时要密封保存,并放在阴凉通风处 |
| D、稀HNO3和活泼金属反应时主要得到氢气 |
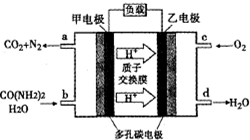 化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于描述正确的是( )
化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于描述正确的是( )| A、电池工作时H+移向负极 |
| B、该电池用的电解质溶液是KOH溶液 |
| C、甲电极反应式为:CO(NH2)2+H2O-6e-═CO2+N2+6H+ |
| D、电池工作时,理论每有净化1mol CO(NH2)2,消耗33.6L O2 |
下列各组物质互为同素异形体的是( )
| A、16O与18O |
| B、金刚石与石墨 |
| C、CH3OH与CH3CH2OH |
D、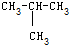 与CH3-CH2-CH2-CH3 与CH3-CH2-CH2-CH3 |
下列物质分类不正确的是( )
| A、氧化铜属于氧化物 |
| B、淀粉属于天然高分子化合物 |
| C、纯碱属于碱类 |
| D、漂白粉属于混合物 |
若要除去MgO中的Al2O3杂质选用的试剂为( )
| A、稀盐酸 | B、NaOH溶液 |
| C、氨水 | D、水 |
在空气中不易变质的是( )
| A、Na2SO3 |
| B、NaHSO4 |
| C、亚硫酸 |
| D、次氯酸 |
NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol乙酸和1mol乙醇充分反应生成的水分子数为NA |
| B、常温常压下,23克NO2分子总数为0.5NA |
| C、标准状况下,2.24L的CCl4中含有的C-Cl键数为0.4NA |
| D、6.8g液态KHSO4中含有0.1NA个阳离子 |
关于二氧化硫的下列叙述,正确的是( )
| A、只具有氧化性 |
| B、只具有还原性 |
| C、酸性KMnO4溶液中通入SO2气体后,紫色消失,说明SO2具有漂白性 |
| D、石蕊溶液中通入SO2后,溶液只变红色但不能消失 |