题目内容
针对实验室制取氨气,下列说法不正确的是( )
| A、发生装置与用KClO3制取O2的装置相同 |
| B、可用排饱和氯化铵溶液的方法收集氨气 |
| C、氨气的验满可以用湿润的红色石蕊试纸或沾有浓盐酸的玻璃棒放于试管口附近 |
| D、所用的铵盐不是NH4NO3,是因为NH4NO3受热易爆炸 |
考点:氨的实验室制法
专题:氮族元素
分析:A.实验室制取氨气选择固固加热装置;
B.排水法适用于不易溶于水且不与水反应的气体来解答;
C.氨气遇湿润的石蕊试纸变蓝或遇浓盐酸产生白烟;
D.NH4NO3受热易爆炸,一般不使用.
B.排水法适用于不易溶于水且不与水反应的气体来解答;
C.氨气遇湿润的石蕊试纸变蓝或遇浓盐酸产生白烟;
D.NH4NO3受热易爆炸,一般不使用.
解答:
解:A.实验室制取氧气,可以用加热氯酸钾或高锰酸钾的方法,要使用加热固体反应物的装置.实验室制取氨气,用的是固体与固体反应,需要加热,实验室制取氧气和氨气的实验装置相同,故A正确;
B.氨气极易溶于水,溶解度太大,NH4Cl无法抑制氨气的溶解,不能用排水法来收集,故B错误;
C.NH3能使湿润的红色石蕊试纸变蓝,故可用湿润的红色石蕊试纸检验氨气,故C正确;
D.NH4NO3受热易爆炸,一般使用NH4Cl或其他非氧化性酸的铵盐,故D正确;
故选B.
B.氨气极易溶于水,溶解度太大,NH4Cl无法抑制氨气的溶解,不能用排水法来收集,故B错误;
C.NH3能使湿润的红色石蕊试纸变蓝,故可用湿润的红色石蕊试纸检验氨气,故C正确;
D.NH4NO3受热易爆炸,一般使用NH4Cl或其他非氧化性酸的铵盐,故D正确;
故选B.
点评:本题考查实验室制取氨气装置、检验、药品选择等知识,注意氨气遇湿润的石蕊试纸变蓝或遇浓盐酸产生白烟是氨气的验满常用方法,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
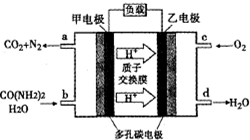 化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于描述正确的是( )
化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于描述正确的是( )| A、电池工作时H+移向负极 |
| B、该电池用的电解质溶液是KOH溶液 |
| C、甲电极反应式为:CO(NH2)2+H2O-6e-═CO2+N2+6H+ |
| D、电池工作时,理论每有净化1mol CO(NH2)2,消耗33.6L O2 |
在空气中不易变质的是( )
| A、Na2SO3 |
| B、NaHSO4 |
| C、亚硫酸 |
| D、次氯酸 |
NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol乙酸和1mol乙醇充分反应生成的水分子数为NA |
| B、常温常压下,23克NO2分子总数为0.5NA |
| C、标准状况下,2.24L的CCl4中含有的C-Cl键数为0.4NA |
| D、6.8g液态KHSO4中含有0.1NA个阳离子 |
下列物质无法通过单质与O2直接化合生成的是( )
| A、Na2O2 |
| B、Al2O3 |
| C、SO3 |
| D、NO |
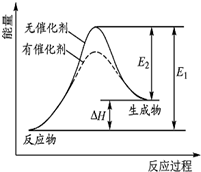 某反应的反应过程中能量变化如右图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如右图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A、该反应为放热反应 |
| B、该反应焓变可表示为△H=-(E1-E2)kJ?mol-1 |
| C、催化剂能降低反应的活化能 |
| D、催化剂能改变反应的焓变 |
在一定条件下,氯气与碘单质以等物质的量进行反应,可得到一种红棕色液体ICl,ICl有很强的氧化性.现有下列两个反应:①2ICl+2Zn=ZnCl2+ZnI2;②ICl+H2O=HCl+HIO.下列关于ICl性质的叙述正确的是( )
| A、反应①中,当转移0.4mol电子时生成13.6g ZnCl2 |
| B、反应①中,ZnCl2是氧化产物,ZnI2是还原产物 |
| C、反应①中,ZnCl2既是氧化产物又是还原产物 |
| D、反应②中,ICl既是氧化剂又是还原剂 |
关于二氧化硫的下列叙述,正确的是( )
| A、只具有氧化性 |
| B、只具有还原性 |
| C、酸性KMnO4溶液中通入SO2气体后,紫色消失,说明SO2具有漂白性 |
| D、石蕊溶液中通入SO2后,溶液只变红色但不能消失 |