题目内容
四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
| 元素 | T | X | Y | Z |
| 性质 结构 信息 | 人体内含量最多的元素,且其单质是常见的助燃剂。 | 单质为双原子分子,分子中含有3对共用电子对,常温下单质气体性质稳定,但其原子较活泼。 | 单质质软、银白色固体、导电性强。 单质在空气中燃烧发出黄色的火焰。 | 第三周期元素的简单离子中半径最小 |
(2)写出Z原子的核外电子排布式 。
(3)Z的最高价氧化物对应水化物的电离方程式 。
(4)元素T与氟元素相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
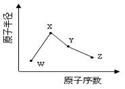
(1)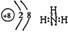 >
>
(2)1S22S22P63S23P1
(3)Al(OH)3 Al3+ + 3OH- 、Al(OH)3
Al3+ + 3OH- 、Al(OH)3 AlO2- + H+ + H2O
AlO2- + H+ + H2O
(4)F bc
解析试题分析:
(1)T元素人体内含量最多,且单质是常见的助燃剂,故T为氧元素。X单质为双原子分子,分子中含有3对共用电子对,常温下单质气体性质稳定,但其原子较活泼。故X为氮元素。Y但在在空气中燃烧发出黄色的火焰,Y为钠元素。Z为第三周期元素的简单离子中半径最小,故Z为铝元素。Y、Z简单离子电子层结构相同,故原子序数越大,离子反应越小,故Y离子>Z离子。
(2)Z为铝元素,故核外电子排布为1S22S22P63S23P1
(3)Al的最高价氧化物对应的水化物为Al(OH)3,其电离分为酸式电离,Al(OH)3 AlO2- + H+ + H2O;碱式电离,Al(OH)3
AlO2- + H+ + H2O;碱式电离,Al(OH)3 Al3+ + 3OH-。
Al3+ + 3OH-。
(4)T元素为氧元素,元素周期表中,非金属性最强的元素为F,故非金属性O<F。a,二者都为分子晶体,单子颜色的深浅主要由相对分子质量大小控制。b,氟气与T的氢化物剧烈反应,产生T的单质,证明,F能够将T的氢化物中置换出来,证明F的非金属性较强。c,氟与T形成的化合物中T元素呈正价态,证明F得电子能力大于T,故F的非金属性较强。d,两元素的单质与氢气化合时的难易程度,或得到氢化物的稳定程度可比较非金属性强弱,与得电子数目无关,故选择bc。
考点:原子结构、元素周期律、非金属性强弱判断。

四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题。
| | W | X | Y | Z |
| 结构或性质 | 最高价氧化物是温室气体,其原子的最外层电子数是次外层电子数的2倍 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 氧化物是常见的两性化合物 | 最高正价与最低负价之和为零 |
(1)Z的氧化物其主要用途为 。在自然界中是 的主要成分。
(2)①下列可作为比较X和W非金属性强弱的依据是 (填序号)。
a.自然界中的含量 b.氢化物的稳定性
c.最高氧化物水化物溶液的酸性 d.单质与酸反应时失去的电子数
②从原子结构的角度解释X的非金属性强于W的原因:电子层数相同,核电荷数X大于W,原子半径X W,所以原子核对最外层电子的吸引力X W,得电子能力X大于W 。
(3)Y的氧化物与X的最高氧化物水化物溶液反应的离子方程式 。
A、B、C、D是原子序数依次增大的短周期主族元素,A、C在元素周期表中的相对位置如图,A元素最外层与次外层上的电子数之差为3,B为地壳中含最最多的金属元素。
| A | |
| | C |
(1)D原子结构示意图为_____________。
(2)将C的低价态氧化物甲通入到D单质的水溶液会使之褪色,体现了甲的________性,写出该反应的离子方程式_____________________。
(3)A的最高价氧化物对应的水化物是乙,现将过量Cu加入到100 mL 8.0 mol/L乙的浓溶液中,充分反应,共收集到6.72L(标准状况)气体,则该气体的成分是_________,还原剂失电子数为_________________。
(4)将两份足量的B单质分别加入到等体积等浓度的盐酸和NaOH溶液中,充分反应生成气体的体积比为__________,若将反应后所得的溶液混合,会生成白色沉淀,发生反应的离子方程式为_____________________________________;B单质表面的氧化膜可用NaOH溶液除去,写出该反应的化学方程式___________________________________。
三氟化氮是一种无色、无味、无毒且不可燃的气体、在半导体加工,太阳能电池和液晶显示器的制造中得到广泛应用。NF3是一种三角锥形分子,键角102°,沸点-l29℃;可在铜的催化作用下由F2和过量NH3反应得到。
(1)写出制备NF3的化学反应方程式: 。
(2)NF3的沸点比NH3的沸点(-33℃)低得多的主要原因是 。
(3)与铜属于同一周期,且未成对电子数最多的元素基态原子核外电子排布式为 。
(4)理论上HF、NaAlO2和NaCl按6:1:2的物质的量之比恰好反应生成HCl、H2O和一种微溶于水的重要原料,该物质含有三种元素,在金属铝的冶炼中有重要作用。该物质为配合物,其中心离子是 ,配位数为 。
(5)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能处于同一族的是 和 。
②T元素最可能是 (填“s”“P” “d”或“ds”等)区元素,位于 族。若T为第2周期元素,F是第3周期元素中原子半径最小的元素,则T与F形成化合物的空间构型为 ,其中心原子的杂化方式为 。