题目内容
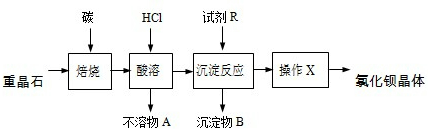
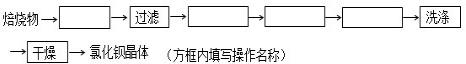
3.某校化学兴趣小组的同学欲测定某种品牌味精中食盐的含量.下面是该小组所做的有关实验步骤:①称取某品牌袋装味精样品10.0g放入烧杯中,并加适量蒸馏水溶解;
②加入足量稀硝酸和硝酸银溶液;
③过滤;
④用蒸馏水洗涤沉淀2-3次;
⑤将沉淀干燥、称量,测得固体质量4.90g.
根据上述实验步骤回答下列问题:
(1)请你在上面的空格内补齐所缺的实验步骤②、③;
(2)实验步骤③所用的玻璃仪器有:漏斗(滤纸)、烧杯、玻璃棒;
(3)检验沉淀是否洗净的方法是:接取最后一次少许洗涤液,加入氯化钠溶液,若无沉淀产生,则说明已洗涤干净
(4)若味精标签上标注:“谷氨酸钠含量≥80.0%,NaCl含量≤20.0%”,则此样品是否合格?合格. (填“合格”,“不合格”).
分析 (1)根据实验原理:氯化钠与硝酸银反应生成氯化银沉淀的质量,计算出氯化钠的质量,再用氯化钠的质量除以袋装味精样品的质量即可;
(2)根据过滤用到的仪器进行分析,
(3)取最后一次洗涤液加入氯化钠溶液看是否有沉淀生成分析判断;
(4)根据方程式AgNO3+NaCl═AgCl↓+NaNO3求出氯化钠的质量,最后求食盐的含量;
解答 解:(1)实验原理:氯化钠与硝酸银反应生成氯化银沉淀的质量,计算出氯化钠的质量,再用氯化钠的质量除以袋装味精样品的质量即可,
故答案为:②加入足量稀硝酸和硝酸银溶液.③过滤;
(2)过滤操作用到的仪器主要有漏斗(滤纸)、烧杯、玻璃棒、铁架台(铁圈);
故答案为:漏斗(滤纸)、烧杯、玻璃棒;
(3)取最后一次洗涤液加入氯化钠溶液看是否有沉淀生成分析,接取最后一次少许洗涤液,加入氯化钠溶液,若无沉淀产生,则说明已洗涤干净;
故答案为:接取最后一次少许洗涤液,加入氯化钠溶液,若无沉淀产生,则说明已洗涤干净;
(4)设:生成4.9g氯化银需要参加反应的氯化钠的质量为X则:
AgNO3+NaCl═AgCl↓+NaNO3
58.5 143.5
X 4.9g
$\frac{58.5}{X}$=$\frac{143.5}{4.9}$
解得X=2.0g;
NaCl含量为$\frac{2.0g}{10.0g}$×100%=20%,此样品是符合产品标示的质量分数,
故答案为:合格.
点评 本题考查了物质组成的分析应用,解答本题的关键是要知道所得固体质量4.9g为生成的氯化银沉淀的质量,再利用氯化银沉淀的质量通过方程式计算出氯化钠的质量,再进一步进行计算,题目难度中等.

练习册系列答案
相关题目
13.已知0.1mol/L的醋酸溶液存在电离平衡:CH3COOH?CH3COO-+H+,下列叙述正确的是( )
| A. | c(H+)+c(CH3COO-)+c(CH3COOH)=0.1mol/L | |
| B. | 加入少量0.1mol/L的盐酸,电离平衡向左移动,c(H+)减小 | |
| C. | 加入少量NaOH固体,电离平衡向右移动,溶液导电性增强 | |
| D. | 加入少量CH3COONa固体,电离平衡不移动,溶液导电性减弱 |
14.下列各组离子在给定条件下一定能大量共存的是( )
| A. | 在c(HCO${\;}_{3}^{-}$)=0.1 mol•L-1的溶液中:NH${\;}_{4}^{+}$、Al3+、Cl-、NO${\;}_{3}^{-}$ | |
| B. | 有大量NO${\;}_{3}^{-}$存在的强酸性溶液中:NH${\;}_{4}^{+}$、Ba2+、Fe3+、Cl- | |
| C. | 由水电离出的c(H+)=1×10-12mol•L-1的溶液中:Na+、Al3+、CH3COO-、I- | |
| D. | 能使pH试纸变红的溶液中:ClO-、S2-、Na+、K+ |
11.某化学研究性学习小组用CO还原Fe2O3,并在实验结束后用磁铁吸出生成的黑色粉末X进行探究.
【探究目的】分析黑色粉末X的组成,并进行相关实验.
【查阅资料】①CO还原Fe2O3的实验中若温度不同、受热不均时会生成Fe3O4,也能被磁铁吸引.
②Fe3O4+8H+═2Fe3++Fe2++4H2O
③Fe+4HNO3(稀)═Fe(NO3)3+NO↑+2H2O
④3Fe3O4+28HNO3(稀)═9Fe(NO3)3+NO↑+14H2O
【实验探究】Ⅰ.定性检验
(1)实验③发生的反应的离子方程式为Fe+Cu2+=Fe2++Cu.
(2)上述实验说明黑色粉末X中含有Fe和Fe3O4.
Ⅱ.定量测定
根据下图所示的实验方案进行实验并记录数据:
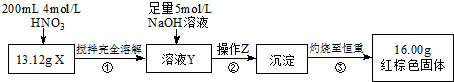
(1)操作Z的名称是过滤.
(2)通过以上数据,得出13.12g黑色粉末X中各成分的物质的量为Fe 0.11mol Fe3O4 0.03mol.
(3)若溶液Y的体积仍为200mL,则溶液Y中c(Fe3+)=1mol/L.
【探究目的】分析黑色粉末X的组成,并进行相关实验.
【查阅资料】①CO还原Fe2O3的实验中若温度不同、受热不均时会生成Fe3O4,也能被磁铁吸引.
②Fe3O4+8H+═2Fe3++Fe2++4H2O
③Fe+4HNO3(稀)═Fe(NO3)3+NO↑+2H2O
④3Fe3O4+28HNO3(稀)═9Fe(NO3)3+NO↑+14H2O
【实验探究】Ⅰ.定性检验
| 编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,注入浓盐酸,微热 | 黑色粉末逐渐溶解,溶液呈黄绿色;有气泡产生 |
| ② | 向试管1中滴加几滴KSCN溶液,振荡 | 溶液出现血红色 |
| ③ | 另取少量黑色粉末X放入试管2中,注入足量硫酸铜溶液,振荡,静置 | 有极少量红色物质析出,仍有较多黑色固体未溶解 |
(2)上述实验说明黑色粉末X中含有Fe和Fe3O4.
Ⅱ.定量测定
根据下图所示的实验方案进行实验并记录数据:

(1)操作Z的名称是过滤.
(2)通过以上数据,得出13.12g黑色粉末X中各成分的物质的量为Fe 0.11mol Fe3O4 0.03mol.
(3)若溶液Y的体积仍为200mL,则溶液Y中c(Fe3+)=1mol/L.
18.某工业废水中含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol•L-1
甲同学与探究该废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少量原溶液,加入KSCN溶液无明显变化.
Ⅲ.另取原溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+(写离子符号).
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O.
(3)将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为3NO2+H2O=2HNO3+NO.
(4)甲同学最终确定原溶液中所含阳离子是Fe2+、Mg2+,阴离子是Cl-、NO3-、SO42-(写离子符号).
(5)另取50mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为0.6g.(保留一位小数)
| 阳离子 | K+、Cu2+、Fe3+、Al3+、Fe2+ |
| 阴离子 | Cl-、CO32-、NO3-、SO42-、SiO32- |
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少量原溶液,加入KSCN溶液无明显变化.
Ⅲ.另取原溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+(写离子符号).
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O.
(3)将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为3NO2+H2O=2HNO3+NO.
(4)甲同学最终确定原溶液中所含阳离子是Fe2+、Mg2+,阴离子是Cl-、NO3-、SO42-(写离子符号).
(5)另取50mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为0.6g.(保留一位小数)
20.下列反应的离子方程式书写正确的是( )
| A. | Ba(OH)2溶液与稀硫酸反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| B. | 用醋酸溶解石灰石:CaCO3+2CH3COOH═Ca2++H2O+CO2↑+2CH3COO- | |
| C. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ | |
| D. | Cu溶于稀硝酸:Cu+2H++NO3=Cu2++NO2↑+H2O |