��Ŀ����
��֪25��ʱ�й�����ĵ���ƽ�ⳣ����
| ���ữѧʽ | CH3COOH | HCN | H2CO3 |
| ����ƽ�ⳣ����25�棩 | 1.8��l0��5 | 4.9��l0��10 | K1=4.3��l0��7 K2=5.6��l0��11 |
A�������ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH��Na2CO3����pH��NaCN����pH��CH3COONa��
B��a mol��L��1 HCN��Һ��b mol��L��1 NaOH��Һ�������ϣ�������Һ��c(Na��)��c(CN��)����aһ��С��b
C������������μ�ˮ������Һ�ĵ����ԡ�����ĵ���ȡ�pH����������С
D��NaHCO3��Na2CO3�����Һ�У�һ����c(Na��)+ c(H��)=c(OH��)+ c(HCO3��) +2c(CO32��)
AD
����

��ϰ��ϵ�д�
�����Ŀ
��֪25��ʱ�й�����ĵ���ƽ�ⳣ����
|
��֪25��ʱ�й�����ĵ���ƽ�ⳣ����
|
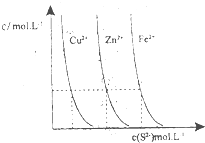 �����ǶԻ�ѧ��Ӧ�仯���̼�������о�����Ҫ��ش����⣺
�����ǶԻ�ѧ��Ӧ�仯���̼�������о�����Ҫ��ش����⣺