题目内容
已知25℃时有关弱酸的电离平衡常数:
|
分析:A.弱酸的电离平衡常数越大,酸性越强,反之酸性越弱,酸性越弱,对应钠盐中酸根离子水解程度越大,溶液的PH越大;
B.氰化钠是强碱弱酸盐,要使其溶液呈中性,则酸的物质的量应该稍微大些;
C.根据电荷守恒判断;
D.冰醋酸属于弱电解质,加水促进电离.
B.氰化钠是强碱弱酸盐,要使其溶液呈中性,则酸的物质的量应该稍微大些;
C.根据电荷守恒判断;
D.冰醋酸属于弱电解质,加水促进电离.
解答:解:A.根据电离平衡常数可知酸性强弱顺序为:CH3COOH>HCN>HCO3-,酸性越弱,对应钠盐中酸根离子水解程度越大,溶液的PH越大,物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa),故A错误;
B.氰化钠是强碱弱酸盐,要使其溶液呈中性,则酸的物质的量应该稍微大些,但溶液的体积未知,无法判断其浓度大小,故B错误;
C.根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故C正确;
D.冰醋酸属于弱电解质,加水促进电离,冰醋酸中逐滴加水,溶液的导电性先增大后减小,pH先减小后增大,醋酸的电离程度逐渐增大,故D错误;
故选C.
B.氰化钠是强碱弱酸盐,要使其溶液呈中性,则酸的物质的量应该稍微大些,但溶液的体积未知,无法判断其浓度大小,故B错误;
C.根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故C正确;
D.冰醋酸属于弱电解质,加水促进电离,冰醋酸中逐滴加水,溶液的导电性先增大后减小,pH先减小后增大,醋酸的电离程度逐渐增大,故D错误;
故选C.
点评:本题考查弱电解质的电离平衡,涉及离子浓度大小比较,做题中注意外界条件对电离平衡的影响,利用电荷守恒、物料守恒解答此类题目.

练习册系列答案
相关题目
已知25℃时有关弱酸的电离平衡常数:
|
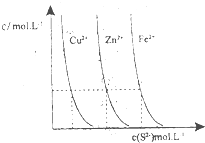 以下是对化学反应变化过程及结果的研究.按要求回答问题:
以下是对化学反应变化过程及结果的研究.按要求回答问题: