题目内容
 以下是对化学反应变化过程及结果的研究.按要求回答问题:
以下是对化学反应变化过程及结果的研究.按要求回答问题:(1)关于能量变化的研究已知:
①2CH3OH(1)+3CO2(g)=2CO2(g)+4H2O(g)△H=-akjmol-
②CH3OH(1)+O2(g)=CO(g)+2H2O(1)△-bkjmol -
③H2O(g)=H2O(1)△H=-ckjmol-
则:2CO(g)+O2(g)=2CO2(g)△H=
(2)关于反应速率和限度的研究
①已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 | CH3COOH | HCN | H2CO |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K1=5.6×10-11 |
②已知2SO2(g)+O2(g)?2SO3(g):△H=-196kjmol,在一个容积为2L的容器中加入2molSO2和lmol O2,在某温度下充分反应,经过30min达到平衡,放出热量176.94kJ.如果用SO2表示该反应的反应速率,则v(SO2)=
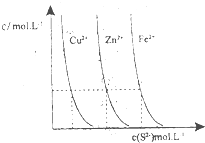
③图为某温度下,CuS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况.如果向三种沉淀中加盐酸,最先溶解的是
(3)关于电化学的研究全钒液流电池是一种新型的绿色环保储能电池.其电池总反应为:VO2++2H++V2+
| 放电 |
| 通电 |
分析:(1)根据盖斯定律,由已知热化学方程式乘以适当系数后进行加减构造目标热化学方程式,反应热也乘以相应的系数作相应的加减,据此计算判断;
(2)①根据溶液的酸碱性以及利用盐类的水解程度比较浓度相同的溶液的pH大小;
②根据2SO2(g)+O2(g)?2SO3(g):△H=-196kJ/mol,经过30min达到平衡,放出热量176.94kJ,求出参加反应的二氧化硫,然后再根据v=
求出v(SO2);
③根据图示某温度下,CuS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况,结合KSP的含义从难溶电解质的溶解平衡角度分析进行解答;
(3)充电时,阳极上得电子发生还原反应;用Pt电极电解CuSO4溶液,发生2CuSO4+2H2O
2Cu+O2↑+2H2SO4,结合转移的电子数来计算解答.
(2)①根据溶液的酸碱性以及利用盐类的水解程度比较浓度相同的溶液的pH大小;
②根据2SO2(g)+O2(g)?2SO3(g):△H=-196kJ/mol,经过30min达到平衡,放出热量176.94kJ,求出参加反应的二氧化硫,然后再根据v=
| △c |
| △t |
③根据图示某温度下,CuS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况,结合KSP的含义从难溶电解质的溶解平衡角度分析进行解答;
(3)充电时,阳极上得电子发生还原反应;用Pt电极电解CuSO4溶液,发生2CuSO4+2H2O
| ||
解答:解:(1)已知:①2CH3OH(1)+3O2(g)═2CO2(g)+4H2O(g)△H=-akJ/mol
②CH3OH(1)+O2(g)=CO(g)+2H2O(1)△=-bkJ/mol
③H2O(g)=H2O(1)△H=-ckJ/mol
由盖斯定律可知,①-②×2+③×4得:
2CO(g)+O2(g)═2CO2(g)△H=-a-[(-b)×2]+(-c)×4=(-a+2b-4c)kJ/mol,
故答案为:-a+2b-4c;
(2)①等物质的量浓度的下列溶液中,
①CH3COONa、②NaCN、③Na2CO3、④NaHCO3溶液都是强碱弱酸盐,水溶液呈碱性,对应酸的酸性越弱水解程度越大,溶液中氢氧根离子浓度越大,PH越大,因H2CO3电离K2=5.6×10-11<HCN的K=4.9×10-10<H2CO3电离K1=4.3×10-7<CH3COOH的1.8×10-5,所以,对应酸根离子的水解程度大小为CH3COO-<HCO3-<CN-<CO32-,所以溶液pH由大到小的顺序③②④①,
故答案为:③②④①;
②2SO2(g)+O2(g)?2 SO3(g),△H=-196kJ/mol,每消耗2mol二氧化硫放出196KJ的热量,经过30min达到平衡,现放出热量176.94kJ,则参加反应的二氧化硫的物质的量为
×2mol=1.81mol,根据v=
,v(SO2)=
=
=0.03mol?L-1?min-1,故答案为:0.03mol?L-1?min-1;
③根据图示某温度下,CuS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况,可知,Ksp(CuS)<Ksp(ZnS)<Ksp(FeS),溶解度CuS<ZnS<FeS,所以,如果向三种沉淀中加盐酸,最先溶解的是FeS,向新生成的ZnS浊液中滴入足量含相同浓度的Cu2+、Fe2+的溶液,振荡后,ZnS沉淀会转化为CuS,
故答案为:FeS;CuS;
(3)根据电池总反应和参加物质的化合价的变化可知,反应中V2+离子被氧化,应是电源的负极,VO2+离子化合价降低,被还原,应是电源的正极反应,充电时,阳极上得电子发生还原反应,阳极反应式为:VO2++H2O=VO2++2H++e-,;
电解硫酸铜时,阴极上是铜离子放电,即Cu2++2e-═Cu,阳极上是氢氧根放电,即4OH-═O2↑+2H2O+4e-,当转移0.1mol电子时,则生成氧气的体积为:
×22.4L/mol=0.56L=560mL,减少的氢氧根的浓度为:
=0.1mol/L,所以电解后氢离子浓度为0.1mol/L,溶液的pH为1,
故答案为:VO2++H2O=VO2++2H++e-;1.
②CH3OH(1)+O2(g)=CO(g)+2H2O(1)△=-bkJ/mol
③H2O(g)=H2O(1)△H=-ckJ/mol
由盖斯定律可知,①-②×2+③×4得:
2CO(g)+O2(g)═2CO2(g)△H=-a-[(-b)×2]+(-c)×4=(-a+2b-4c)kJ/mol,
故答案为:-a+2b-4c;
(2)①等物质的量浓度的下列溶液中,
①CH3COONa、②NaCN、③Na2CO3、④NaHCO3溶液都是强碱弱酸盐,水溶液呈碱性,对应酸的酸性越弱水解程度越大,溶液中氢氧根离子浓度越大,PH越大,因H2CO3电离K2=5.6×10-11<HCN的K=4.9×10-10<H2CO3电离K1=4.3×10-7<CH3COOH的1.8×10-5,所以,对应酸根离子的水解程度大小为CH3COO-<HCO3-<CN-<CO32-,所以溶液pH由大到小的顺序③②④①,
故答案为:③②④①;
②2SO2(g)+O2(g)?2 SO3(g),△H=-196kJ/mol,每消耗2mol二氧化硫放出196KJ的热量,经过30min达到平衡,现放出热量176.94kJ,则参加反应的二氧化硫的物质的量为
| 176.94KJ |
| 196KJ |
| △c |
| △t |
| △c |
| △t |
| 1.81mol | ||
|
③根据图示某温度下,CuS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况,可知,Ksp(CuS)<Ksp(ZnS)<Ksp(FeS),溶解度CuS<ZnS<FeS,所以,如果向三种沉淀中加盐酸,最先溶解的是FeS,向新生成的ZnS浊液中滴入足量含相同浓度的Cu2+、Fe2+的溶液,振荡后,ZnS沉淀会转化为CuS,
故答案为:FeS;CuS;
(3)根据电池总反应和参加物质的化合价的变化可知,反应中V2+离子被氧化,应是电源的负极,VO2+离子化合价降低,被还原,应是电源的正极反应,充电时,阳极上得电子发生还原反应,阳极反应式为:VO2++H2O=VO2++2H++e-,;
电解硫酸铜时,阴极上是铜离子放电,即Cu2++2e-═Cu,阳极上是氢氧根放电,即4OH-═O2↑+2H2O+4e-,当转移0.1mol电子时,则生成氧气的体积为:
| 0.1mol |
| 4 |
| 0.1mol |
| 1.0L |
故答案为:VO2++H2O=VO2++2H++e-;1.
点评:本题比较综合,考查了盖斯定律的应用、热化学方程式的意义、沉淀转化的原理应用、电化学等知识,构造目标热化学方程式、掌握难溶电解质的溶解平衡及沉淀转化的本质、掌握原电池与电解池的工作原理是解题的关键,题目难度较大.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
近年来,我国部分地区多次陷入严重雾霾之中,其中一个重要的原因是我国的能源消费结构以燃煤为主,改变煤的利用方式可减少环境污染.以下是对煤进行处理的方法:
(1)将水蒸气通过红热的碳即可产生水煤气,其反应为C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ?mol-1,
①该反应在 下能自发进行(填“高温”或“低温”);
②煤气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为 .(已知:H2S Ka1=9.1×10-8;Ka2=1.1×10-12 H2CO3 Ka1=4.30×10-7;Ka2=5.61×10-11)
(2)利用水煤气作为合成气,在同一个容器中,选择双催化剂,经过如下三步反应,最终合成二甲醚,此工艺称之为“一步法”合成二甲醚.
①一步法合成二甲醚:3H2(g)+3CO(g)=CH3OCH3(g)+CO2 (g)△H= .
②该反应在一定条件下的密闭容器中达到平衡后,为同时提高化学反应速率和二甲醚的产率,可以采取的措施是 (填字母代号).
a.降低温度 b.缩小容器体积 c.加入催化剂
d.增加H2的浓度 e.分离出二甲醚
(3)控制反应条件,水煤气作为合成气也可以用来合成甲醇.在相同条件下合成二甲醚和合成甲醇的原料转化率随氢碳比的变化如图所示:
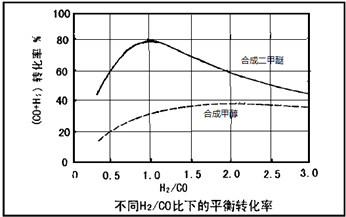
①合成二甲醚的最佳H2/CO比为 .对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作KP),写出“一步法”合成二甲醚的KP= ,提高H2/CO比,则KP (填“变大”、“变小”或“不变”)
②以水煤气作为原料气,在相同条件下一步法合成二甲醚的转化率为什么明显高于合成甲醇的转化率 .
(1)将水蒸气通过红热的碳即可产生水煤气,其反应为C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ?mol-1,
①该反应在
②煤气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为
(2)利用水煤气作为合成气,在同一个容器中,选择双催化剂,经过如下三步反应,最终合成二甲醚,此工艺称之为“一步法”合成二甲醚.
| 反应过程 | 化学方程式 | △H(kJ?mol-1) |
| 甲醇合成反应 | 2H2(g)+CO(g)=CH3OH(g) | -90.8 |
| 水煤气变换反应 | CO(g)+H2O(g)═CO2(g)+H2(g) | -41.3 |
| 甲醇脱水反应 | 2CH3OH(g)=CH3OCH3(g)+H2O(g) | -23.5 |
②该反应在一定条件下的密闭容器中达到平衡后,为同时提高化学反应速率和二甲醚的产率,可以采取的措施是
a.降低温度 b.缩小容器体积 c.加入催化剂
d.增加H2的浓度 e.分离出二甲醚
(3)控制反应条件,水煤气作为合成气也可以用来合成甲醇.在相同条件下合成二甲醚和合成甲醇的原料转化率随氢碳比的变化如图所示:

①合成二甲醚的最佳H2/CO比为
②以水煤气作为原料气,在相同条件下一步法合成二甲醚的转化率为什么明显高于合成甲醇的转化率
以下是对化学反应变化过程及结果的研究。按要求回答问题:
Ⅰ.关于反应速率和限度的研究
(1)已知25℃时有关弱酸的电离平衡常数:
弱酸化学式 | CH3COOH | HCN | H2CO3 |
电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
则等物质的量浓度的①CH3COONa、②NaCN、③Na2CO3、④NaHCO3溶液的pH由大到小的顺序为__________(填编号)。
(2)已知2SO2(g)+O2(g)??2SO3(g) ΔH=-196.6 kJ·mol-1,在一个容积为2 L的容器中加入2 mol SO2和1 mol O2,在某温度下充分反应,经过30 min达到平衡,放出热量176.94 kJ。如果用SO2表示该反应的反应速率,则v(SO2)=________。
(3)下图为某温度下,CuS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况。如果向三种沉淀中加盐酸,最先溶解的是________。

向新生成的ZnS浊液中滴入足量含相同浓度的Cu2+、Fe2+的溶液,振荡后,ZnS沉淀会转化为________(填化学式)沉淀。
Ⅱ.关于电化学的研究
全钒液流电池是一种新型的绿色环保储能电池。其电池总反应为:VO2++2H++V2+ V3++VO2++H2O。则充电时阳极反应式为__________________________,用此电池电解1 L 1 mol·L-1的CuSO4溶液,当转移0.1 mol电子时,溶液的pH=________(不考虑溶液体积变化)。
V3++VO2++H2O。则充电时阳极反应式为__________________________,用此电池电解1 L 1 mol·L-1的CuSO4溶液,当转移0.1 mol电子时,溶液的pH=________(不考虑溶液体积变化)。
 Cu(OH)2+2H+
Cu(OH)2+2H+
