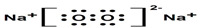题目内容
10.下列各组离子一定能大量共存的是( )| A. | 在强酸性溶液中:NH4+、Ca2+、NO3-、HCO3- | |
| B. | 强碱性溶液中:NH4+、Al3+、HCO3-、NO3- | |
| C. | 在强碱溶液中:Na+、K+、Cl-、CO32- | |
| D. | 在无色溶液中:K+、H+、Cl-、MnO4- |
分析 A.与H+反应的离子不能大量共存;
B.与OH-反应的离子不能大量共存
C.离子之间不发生任何反应;
D.有颜色的离子不能大量共存.
解答 解:A.HCO3-与H+反应反应,不能大量共存,故A错误;
B.NH4+、Al3+、HCO3-与OH-反应,不能大量共存,故B错误;
C.离子之间不发生任何反应,可大量共存,故C正确;
D.MnO4-有颜色的离子,不符合题目无色要求,故D错误.
故选C.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
20.下列各组离子,在指定的环境中一定能大量共存的是( )
| A. | 常温下,在c(H+)/c(OH-)=1×1012的溶液中:I-、Cl-、NO${\;}_{3}^{-}$、Na+ | |
| B. | 在能使石蕊变红色的溶液中:Na+、S2-、SO${\;}_{4}^{2-}$、CO${\;}_{3}^{2-}$ | |
| C. | 在加入铝粉能产生H2的溶液中:NH${\;}_{4}^{+}$、Na+、NO${\;}_{3}^{-}$、Cl- | |
| D. | 常温下由水电离出的c(H+)=1×10-12 mol•L-1的溶液中:K+、Cl-、NO${\;}_{3}^{-}$、Na+ |
1.下列离子方程式书写正确的是( )
| A. | 酸碱中和反应均可表示为:OH-+H+═H2O | |
| B. | 碳酸氢钠溶液与烧碱溶液混合:HCO3-+OH-═CO32-+H2O | |
| C. | 硫酸和氢氧化钡溶液反应:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| D. | 铜片插入硝酸银溶液中:Cu+Ag+═Ag+Cu2+ |
18.用NA表示阿伏德罗常数,下列叙述正确的是( )
| A. | 通常状况下,1 NA 个CO2分子占有的体积为22.4 L | |
| B. | 标准状况下,22.4 L H2O含有的分子数为1 NA | |
| C. | 常温常压下,1.06 g Na2CO3含有的Na+数为0.02 NA | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为1 NA |
15.关于氧化还原反应10AgF+5Cl2+5H2O═9□+AgClO3+10HF+O2的说法不正确的是( )
| A. | 每生成1mol O2,该反应转移电子的物质的量是9mol | |
| B. | 该反应中Cl2既是氧化剂,又是还原剂 | |
| C. | □上的物质是AgCl | |
| D. | 参加反应的Cl2有$\frac{4}{9}$被水还原 |
2.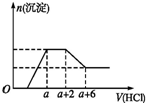 某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+.当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀物质的量随盐酸的体积变化如图所示,下列说法正确的是( )
某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+.当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀物质的量随盐酸的体积变化如图所示,下列说法正确的是( )
 某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+.当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀物质的量随盐酸的体积变化如图所示,下列说法正确的是( )
某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+.当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀物质的量随盐酸的体积变化如图所示,下列说法正确的是( )| A. | 原溶液一定含有Na2SO4 | |
| B. | 反应最后形成的溶液中的溶质为NaCl | |
| C. | 原溶液中一定含有的阴离子是OH-、CO32-、AlO2-、SiO32- | |
| D. | 原溶液中含有CO32-与AlO2-的物质的量之比为1:1 |
19.下列化学方程式中△H的值能表示可燃物的燃烧热的是( )
| A. | H2(g)+Cl2(g)═2HCl(g)△H=-184.6kJ/mol | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3kJ/mol | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol | |
| D. | CO(g)+O2(g)═CO2(g)△H=-258 kJ/mol |