题目内容
14.在某无色透明的且能使紫色石蕊试剂变红的溶液中,能大量共存的离子组是( )| A. | Na+、SO42-、HCO3- | B. | NH4+、SO42-、NO3- | C. | Cu2+、ClO-、NO3- | D. | K+、OH-、Cl- |
分析 溶液无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,能使紫色石蕊试剂变红的溶液中存在大量氢离子,
A.碳酸氢根离子与氢离子反应;
B.三种离子之间不反应,都不与氢离子反应,且为无色溶液;
C.铜离子为有色离子,次氯酸根离子与氢离子反应;
D.氢离子与氢氧根离子反应.
解答 解:无色溶液可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,能使紫色石蕊试剂变红的溶液中存在大量氢离子,
A.HCO3-与氢离子反应生成二氧化碳气体,在溶液中不能大量共存,故A错误;
B.NH4+、SO42-、NO3-之间不反应,都不与氢离子反应,且为无色溶液,在溶液中能够大量共存,故B正确;
C.Cu2+为有色离子,ClO-与氢离子反应生成次氯酸,在溶液中不能大量共存,故C错误;
D.OH-与氢离子反应生成水,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的正误判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
相关题目
4.常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如表所示:
(1)从甲组情况分析,从a值如何大小判断HA是强酸还是弱酸?a=7时,HA是强酸;a>7时,HA是弱酸.
(2)乙组混合溶液中c(A-)和c(Na+)的大小关系是C.
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+).
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):
c(Na+)-c(A-)=10-4-10-10 mol•L-1.
(5)某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B═H++HB-
HB-?H++B2-.
在0.1mol•L-1的Na2B溶液中,下列粒子浓度关系式正确的是AC.
A.c(B2-)+c(HB-)=0.1mol•L-1
B.c(B2-)+c(HB-)+c(H2B)=0.1mol•L-1
C.c(OH-)=c (H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
| 实验 编号 | HA的物质的量 浓度(mol•L-1) | NaOH的物质的量 浓度(mol•L-1) | 混合后溶 液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
(2)乙组混合溶液中c(A-)和c(Na+)的大小关系是C.
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+).
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):
c(Na+)-c(A-)=10-4-10-10 mol•L-1.
(5)某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B═H++HB-
HB-?H++B2-.
在0.1mol•L-1的Na2B溶液中,下列粒子浓度关系式正确的是AC.
A.c(B2-)+c(HB-)=0.1mol•L-1
B.c(B2-)+c(HB-)+c(H2B)=0.1mol•L-1
C.c(OH-)=c (H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
5.下列电离方程式错误的是( )
| A. | CaCl2=Ca2++2Cl- | B. | Na2SO4=Na++2SO42- | ||
| C. | HNO3=H++NO${\;}_{3}^{-}$ | D. | Na2CO3=2Na++CO32 |
2.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 0.1mol•L-1CH3COONa溶液与0.1 mol•L-1CH3COOH溶液等体积混合(pH=4.75):c (CH3COO-)+c (CH3COOH)=2 c(Na+) | |
| C. | 0.1mol•L-1CH3COONa溶液与0.1 mol•L-1 HCl溶液混合至pH=7:c(Na+)>c(Cl-)=c(CH3COOH)>c(CH3COO-) | |
| D. | 0.1mol•L-1 Na2CO3溶液与0.1 mol•L-1 NaHCO3溶液等体积混合:c (HCO${\;}_{3}^{-}$)+2c (H+)+3c (H2CO3)=c(CO${\;}_{3}^{2-}$)+2c(OH-) |
19.下列有关物质的性质或应用正确的是( )
| A. | Na2O用作呼吸面具的供氧剂 | |
| B. | 氧化铝常用于制造耐火材料 | |
| C. | 米汤可检验碘盐中的碘酸钾 | |
| D. | 食品包装袋内放入生石灰可以防止食品因氧化而变质 |
4.甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上一般采用下列两种反应合成甲醇.
反应Ⅰ:CO(g)+2H2(g)?CH3OH(g)△H1
反应Ⅱ:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K):
(1)在一定条件下将2mol CO和6mol H2充入2L的密闭容器中发生反应Ⅰ,5min后测得
c(CO)=0.4mol/L,计算可得此段时间的反应速率(用H2表示)为0.24mol/(L•min).
(2)由表中数据判断△H1<0 (填“>”、“<”或“=”);
反应CO2(g)+H2(g)?CO(g)+H2O(g)△H3=△H2-△H1 (用△H1和△H2表示).
(3)若容器容积不变,则下列措施可提高反应Ⅰ中CO转化率的是b (填字母序号).
a.充入CO,使体系总压强增大 b.将CH3OH(g)从体系中分离
c.充入He,使体系总压强增大 d.使用高效催化剂
(4)写出反应Ⅱ的化学平衡常数表达式:KⅡ=$\frac{c(CH{\;}_{3}OH)•c(H{\;}_{2}O)}{c(CO{\;}_{2})•c{\;}^{3}(H{\;}_{2})}$;保持恒温恒容,将反应Ⅱ的平衡体系中各物质浓度均增大为原来的2倍,则化学平衡正向移动(填“正向”、“逆向”或“不”),平衡常数KⅡ不变(填“变大”、“变小”或“不变”).
反应Ⅰ:CO(g)+2H2(g)?CH3OH(g)△H1
反应Ⅱ:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K):
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.0 | 0.27 | 0.012 |
c(CO)=0.4mol/L,计算可得此段时间的反应速率(用H2表示)为0.24mol/(L•min).
(2)由表中数据判断△H1<0 (填“>”、“<”或“=”);
反应CO2(g)+H2(g)?CO(g)+H2O(g)△H3=△H2-△H1 (用△H1和△H2表示).
(3)若容器容积不变,则下列措施可提高反应Ⅰ中CO转化率的是b (填字母序号).
a.充入CO,使体系总压强增大 b.将CH3OH(g)从体系中分离
c.充入He,使体系总压强增大 d.使用高效催化剂
(4)写出反应Ⅱ的化学平衡常数表达式:KⅡ=$\frac{c(CH{\;}_{3}OH)•c(H{\;}_{2}O)}{c(CO{\;}_{2})•c{\;}^{3}(H{\;}_{2})}$;保持恒温恒容,将反应Ⅱ的平衡体系中各物质浓度均增大为原来的2倍,则化学平衡正向移动(填“正向”、“逆向”或“不”),平衡常数KⅡ不变(填“变大”、“变小”或“不变”).
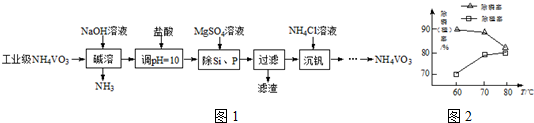
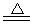 H2SiO3↓+2OH-(或者SiO32-+3H2O
H2SiO3↓+2OH-(或者SiO32-+3H2O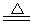 H4SiO4↓+2OH-)(用离子方程式表示).
H4SiO4↓+2OH-)(用离子方程式表示).