题目内容
【题目】试从化学键的角度理解化学反应中的能量变化。(以2H2+O2===2H2O为例说明),已知:E反表示反应物(2H2+O2)所具有的总能量,E生表示生成物(2H2O)所具有的总能量。又知:拆开1moL H2中的化学键需要吸收436kJ能量,拆开1moL O2中的化学键需要吸收496kJ能量,形成水分子中的1moLH—O键能够释放463KJ能量。
⑴从宏观角度看:反应物所具有的总能量高于生成物所具有的总能量,所以该反应要______(填“吸收”或“放出”)能量,能量变化值的大小△E=_________(用E反和E生表示)
⑵从微观角度看:断裂反应物中的化学键吸收的总能量为E吸=______KJ;形成生成物中的化学键放出的总能量为=______KJ。E吸______E放(填“>”或“<”),所以该反应要_____(填“吸收”或“放出”)能量,能量变化值的大小△E=____ KJ(填数值)
⑶由图可知,化学反应的本质是________________________________化学反应中能量变化的主要原因是________________(从总能量说明)
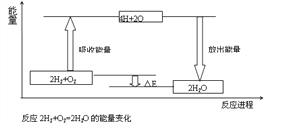
【答案】 放出 E生—E反 1368 1852 < 放出 484 旧化学键的断裂,新化学键的形成 反应物总能量与生成物总能量的不同。
【解析】⑴从宏观角度看:反应物所具有的总能量高于生成物所具有的总能量,所以该反应要放出能量,能量变化值的大小△E=E生 - E反。
⑵从微观角度看:2mol H2和1mol O2反应生成 2mol H2O的反应过程中,断裂反应物中的化学键吸收的总能量为E吸=436KJ![]() +496KJ=1368KJ;形成生成物中的化学键放出的总能量为= 463KJ
+496KJ=1368KJ;形成生成物中的化学键放出的总能量为= 463KJ![]() 1852KJ。E吸<E放,所以该反应要放出能量,能量变化值的大小△E=484KJ。
1852KJ。E吸<E放,所以该反应要放出能量,能量变化值的大小△E=484KJ。
⑶由图可知,化学反应的本质是旧化学键的断裂,新化学键的形成,化学反应中能量变化的主要原因是反应物总能量与生成物总能量的不同。



