题目内容
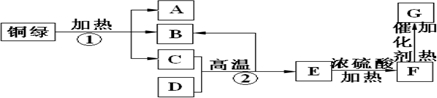
已知A~G均为中学化学常见的物质,A、B、C、F、G为氧化物,D、E为单质.C、D为黑色固体.它们之间有如下图所示的转化关系:
(1)写出下列反应的化学方程式:
① ② ③E→F:
(2)写出下列反应的化学方程式:
④湿法炼铜: ⑤实验室制备B: ⑥E与氯化铁溶液反应: .

(1)写出下列反应的化学方程式:
①
(2)写出下列反应的化学方程式:
④湿法炼铜:
考点:无机物的推断,铜金属及其重要化合物的主要性质
专题:推断题,几种重要的金属及其化合物
分析:铜绿为Cu2(OH)2CO3,分解生成CuO、H2O、CO2,A、B、C、F、G为氧化物,D、E为单质.C、D为黑色固体,结合转化关系可知,A为H2O,B为CO2,C为CuO,D为C,E为Cu,F为SO2,G为SO3,然后结合物质的性质及化学用语来解答.
解答:
解:铜绿为Cu2(OH)2CO3,分解生成CuO、H2O、CO2,A、B、C、F、G为氧化物,D、E为单质.C、D为黑色固体,结合转化关系可知,A为H2O,B为CO2,C为CuO,D为C,E为Cu,F为SO2,G为SO3,
(1)反应①为Cu2(OH)2CO3
2CuO+H2O+CO2↑,反应②为2CuO+C
2Cu+CO2↑,反应③E→F为Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,
故答案为:Cu2(OH)2CO3
2CuO+H2O+CO2↑;2CuO+C
2Cu+CO2↑;Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
(2)④湿法炼铜的反应为Fe+CuSO4═FeSO4+Cu,⑤实验室制备B的反应为CaCO3+2HCl=CaCl2+H2O+CO2↑,⑥E与氯化铁溶液反应2FeCl3+SO2+2H2O═H2SO4+2FeCl2+2HCl,故答案为:Fe+CuSO4═FeSO4+Cu;CaCO3+2HCl=CaCl2+H2O+CO2↑;2FeCl3+SO2+2H2O═H2SO4+2FeCl2+2HCl.
(1)反应①为Cu2(OH)2CO3
| ||
| ||
| ||
故答案为:Cu2(OH)2CO3
| ||
| ||
| ||
(2)④湿法炼铜的反应为Fe+CuSO4═FeSO4+Cu,⑤实验室制备B的反应为CaCO3+2HCl=CaCl2+H2O+CO2↑,⑥E与氯化铁溶液反应2FeCl3+SO2+2H2O═H2SO4+2FeCl2+2HCl,故答案为:Fe+CuSO4═FeSO4+Cu;CaCO3+2HCl=CaCl2+H2O+CO2↑;2FeCl3+SO2+2H2O═H2SO4+2FeCl2+2HCl.
点评:本题考查无机物的推断,为高频考点,把握铜绿的分解反应及图中转化为推断的关系,侧重Cu及其化合物、S及其化合物性质的考查,注意物质的性质及制备,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列叙述正确的是( )
| A、加入铝粉能产生H2的溶液中可能大量共存的离子组:NH4+、Fe2+、SO42-、NO3- |
| B、碳酸氢钠溶液中离子浓度的大小关系c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-) |
| C、碳酸钠溶液中离子浓度的关系2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| D、向Ca(ClO)2溶液中通入少量CO2的离子方程式:2ClO-+CO2+H2O═2HClO+CO32- |
用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是( )
| A、加热 |
| B、用98%的浓硫酸代替稀硫酸 |
| C、滴加少量硫酸铜溶液 |
| D、不用铁片改用铁粉 |
下列有关离子键、共价键的叙述中正确的是( )
| A、离子化合物中只存在离子键,没有共价键 |
| B、构成单质分子的粒子中一定含有共价键 |
| C、共价化合物分子中一定不存在离子键 |
| D、仅由非金属元素组成的化合物中一定不含离子键 |
除去甲烷气体中含有的少量乙烯,最好选用下列试剂中的( )
| A、蒸馏水 |
| B、溴的四氯化碳溶液 |
| C、浓硫酸 |
| D、酸性KMnO4溶液 |
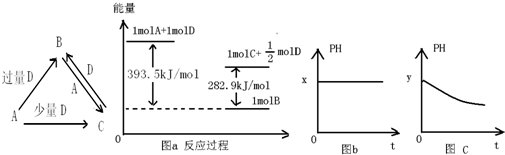
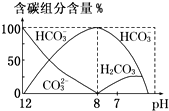 在含有弱电解质的溶液中,往往有多个化学平衡共存.
在含有弱电解质的溶液中,往往有多个化学平衡共存.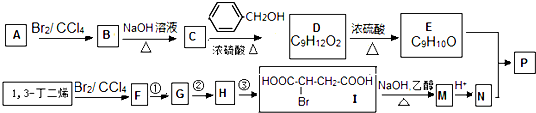
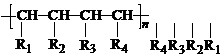 nCH=CH+nCH=CH
nCH=CH+nCH=CH