题目内容
5.硅是信息产业、太阳能电池光电转化的基础材料.锌还原四氯化硅是一种有着良好应用前景的制备硅的方法,该制备过程示意如下: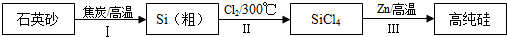
(1)焦炭在过程Ⅰ中作还原剂.
(2)过程Ⅱ中的Cl2用电解饱和食盐水制备,制备Cl2的化学方程式是2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑.
(3)整个制备过程必须严格控制无水.
①SiCl4遇水剧烈水解生成SiO2和一种酸,反应的化学方程式是SiCl4+2H2O═SiO2+4HCl.
②干燥Cl2时,从有利于充分干燥和操作安全的角度考虑,需将约90℃的潮湿氯气先冷却至12℃,然后再通入到浓H2SO4中.冷却的作用是使水蒸气冷凝减少进入浓硫酸的水量保持持续的吸水性并降低放出的热量.
(4)Zn还原SiCl4的反应如下:
反应1:400℃~756℃,SiCl4(g)+2Zn(l) Si(s)+2ZnCl2(l)△H1<0
反应2:756℃~907℃,SiCl4(g)+2Zn(l) Si(s)+2ZnCl2(g)△H2<0
反应3:907℃~1410℃,SiCl4(g)+2Zn(g) Si(s)+2ZnCl2(g)△H3<0
①对于上述三个反应,下列说法合理的是bcd.
a.升高温度会提高SiCl4的转化率 b.还原过程需在无氧的气氛中进行
c.增大压强能提高反应的速率 d.Na、Mg可以代替Zn还原SiCl4
②实际制备过程选择“反应3”,选择的理由是温度高反应速率快;与前两个反应比较更易于使硅分离使化学平衡向右移动提高转化率.
③已知Zn(l)═Zn(g)△H=+116KJ/mol.若SiCl4的转化率均为90%,每投入1mol SiCl4,“反应3”比“反应2”多放出208.8kJ的热量.
(5)用硅制作太阳能电池时,为减弱光在硅表面的反射,采用化学腐蚀法在其表面形成粗糙的多孔硅层.腐蚀剂常用稀HNO3和HF的混合液.硅表面首先形成SiO2,最后转化为H2SiF6.用化学方程式表示SiO2转化为H2SiF6的过程SiO2+6HF═H2SiF6+2H2O.
分析 (1)在氧化还原反应中,化合价升高的元素发生还原反应;
(2)电解饱和食盐水的方法制备氯气,阳极,溶液中氯离子失电子发生氧化反应生成氯气,阴极,溶液中氢离子得到电子发生还原反应,生成氢气;
(3)①SiCl4遇水剧烈水解生成SiO2和一种酸,据此信息找出反应物和生成物,结合质量守恒书写化学方程式;
②水的沸点为100℃,浓硫酸具有吸水性,溶于水放热,据此解答;
(4)①△H<0表示放热,根据平衡移动的原理解答;
②反应2与反应1比较,反应2产物为固体和气体比反应1更易于分离,反应3与反应2比较,温度高,反应速率更快;
③根据盖斯定律可以计算化学反应的焓变;
(5)氟化氢跟二氧化硅反应生成四氟化硅和水,四氟化硅和氟化氢直接反应生成H2SiF6.
解答 解:(1)在过程Ⅰ中发生反应2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑中,C从0价变为一氧化碳中的+2价,发生氧化反应是还原剂,故答案为:还原;
(2)电解饱和食盐水的方法制备氯气,阳极,溶液中氯离子失电子发生氧化反应生成氯气,2Cl--2e=Cl2↑,阴极,溶液中氢离子得到电子发生还原反应,生成氢气,2H++2e-═H2↑,总的反应为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑,
故答案为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑;
(3)①根据SiCl4遇水剧烈水解生成SiO2和一种酸信息,反应物是SiCl4和水,生成物为二氧化硅,根据氧原子守恒,水分子前的系数为2,根据氢原子和氯原子守恒,另一产物为氯化氢,氯化氢前的系数为4,可知化学反应方程式为SiCl4+2H2O═SiO2+4HCl,
故答案为:SiCl4+2H2O═SiO2+4HCl;
②干燥Cl2时,从有利于充分干燥和操作安全的角度考虑,需将约90℃的潮湿氯气先冷却至12℃,此时使水蒸气冷凝,然后再通入到浓H2SO4中,进入浓硫酸的水量少了,保证浓硫酸的良好吸水性,水和浓硫酸作用放热,所以进入硫酸的水少了,能降低放出的热量,
故答案为:使水蒸气冷凝减少进入浓硫酸的水量保持持续的吸水性并降低放出的热量;
(4)①对于三个反应,反应热都是△H<0表示放热,
a.升高温度,平衡向吸热的方向移动,所以会降低SiCl4的转化率,故a错误;
b.Si遇氧气在高温的条件下反应生成二氧化硅,所以还原过程需在无氧的气氛中进行,b正确;
c.有气体参加的反应,增大压强,能加快反应的速率,对于三个反应,都有气体参与,所以增大压强,能提高反应的速率,故c正确;
d.Na、Mg都是还原性比较强的金属,可以代替Zn还原SiCl4,故d正确;
故答案为:bcd;
②反应2与反应1比较,反应2产物为固体和气体比反应1更易于分离,反应3与反应2比较,反应物都为气态,温度高,反应速率更快,所以实际制备过程选择“反应3”,温度高反应速率快;与前两个反应比较更易于使硅分离使化学平衡向右移动提高转化率,
故答案为:温度高反应速率快;与前两个反应比较更易于使硅分离使化学平衡向右移动提高转化率;
③每投入1mol SiCl4,有2molZn参加反应,“反应3”与“反应2”比较,反应2中锌为液态,根据Zn(l)═Zn(g)△H=+116KJ/mol,若SiCl4的转化率均为90%,“反应3”比“反应2”多放出116KJ/mol×2×90%=208.8KJ,
故答案为:208.8;
(5)二氧化硅和氢氟酸:SiO2+4HF=SiF4↑+2H2O;SiF4+2HF=H2SiF6,所以用稀HNO3和HF的混合液,硅表面首先形成SiO2,最后转化为H2SiF6的化学方程式为SiO2+6HF═H2SiF6+2H2O,
故答案为:SiO2+6HF═H2SiF6+2H2O.
点评 本题考查锌还原四氯化硅制备硅,涉及化学平衡移动、电解等知识,掌握平衡移动原理的运用,掌握硅及其化合物的性质是解答的关键,题目难度中等.

| A. | (b-2a)bmol•L-1 | B. | $\frac{(b-2a)}{2}$bmol•L-1 | C. | (2b-a)bmol•L-1 | D. | $\frac{(2b-a)}{2}$bmol•L-1 |

相关化合物的物理常数
| 物质 | 相对分子质量 | 密度(g/cm-3) | 沸点/℃ |
| 苯酚 | 94 | 1.0722 | 182 |
| 丙酮 | 58 | 0.7898 | 56.5 |
| 异丙苯 | 120 | 0.8640 | 153 |
(1)反应①和②分别在装置A和C中进行(填装置符号).
(2)反应②为放热(填“放热”或“吸热”)反应.反应温度控制在50-60℃,温度过高的安全隐患是温度过高会导致爆炸.
(3)在反应器A中通入的X是氧气或空气.
(4)在分解釜C中加入的Y为少量浓硫酸,其作用是催化剂,优点是用量少,缺点是腐蚀设备.
(5)中和釜D中加入的Z最适宜的是c(填编号.已知苯酚是一种弱酸)
a.NaOH b.CaCO3 c.NaHCO3 d.CaO
(6)蒸馏塔F中的馏出物T和P分别为丙酮和苯酚,判断的依据是丙酮的沸点低于苯酚.
(7)用该方法合成苯酚和丙酮的优点是原子利用率高.
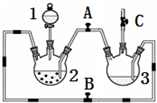 某化学兴趣小组拟用图装置制备氢氧化亚铁并观察其颜色.提供化学药品:铁屑、稀硫酸、氢氧化钠溶液.
某化学兴趣小组拟用图装置制备氢氧化亚铁并观察其颜色.提供化学药品:铁屑、稀硫酸、氢氧化钠溶液.(1)稀硫酸应放在1中(填写仪器名称).
(2)本实验通过控制A、B、C三个开关,将仪器中的空气排尽后,再关闭开关B、打开开关AC就可观察到氢氧化亚铁的颜色.试分析实验开始时排尽装置中空气的理由防止生成的氢氧化亚铁被氧化
(3)在FeSO4溶液中加入(NH4)2SO4固体可制备摩尔盐晶体[(NH4)2SO4•FeSO4•6H2O](相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇.
①为洗涤(NH4)2SO4•FeSO4•6H2O粗产品,下列方法中最合适的是D
A.用冷水洗 B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗 D.用90%的乙醇溶液洗
②为了测定产品的纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol•L-1的酸性KMnO4溶液滴定.每次所取待测液体积均为25.00mL,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
滴定终点的现象是最后一滴滴入,溶液由无色变为浅紫色,且30s不变色
通过实验数据计算的该产品纯度为$\frac{980c}{a}$×100%(用字母ac表示).
上表中第一次实验中记录数据明显大于后两次,其原因可能是BC
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低.
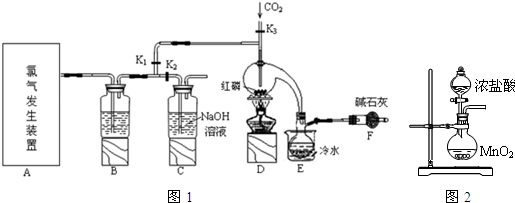
已知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5.PCl3遇O2会生成POCl3(三氯氧磷),POCl3溶于PCl3,PCl3遇水会强烈水解生成H3PO3和HCl.PCl3、POCl3的熔沸点见表.
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
(1)B中所装试剂是浓硫酸,F中碱石灰的作用是吸收多余的Cl2,防止空气中的水蒸气进入烧瓶与PCl3反应.
(2)实验时,检查装置气密性后,向D装置的曲颈甑中加入红磷,打开K3通入干燥的CO2,一段时间后,关闭K3,加热曲颈甑至上部有黄色升华物出现时通入氯气,反应立即进行.通干燥CO2的作用是排尽装置中的空气,防止红磷自燃,
(3)实验制得的粗产品中常含有POCl3、PCl5等.加入红磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.
(4)C装置中的K1、K2的设计也出于类似的目的,为了达到这一实验目的,实验时与K1、K2有关的操作是先关闭K1,打开K2,等B中溶液上方充满黄绿色气体后,打开K1,关闭K2.
(5)实验后期关闭K1,打开K2,将气体通入C装置中发生反应,反应后的溶液为X.某同学设计实验来确定溶液X中含有的某些离子,请补充完成实验步骤和现象.
| 实验步骤 | 实验现象 | 实验结论 |
| ① | 溶液X中含有Na+ | |
| ② | 溶液X中含有Cl- |
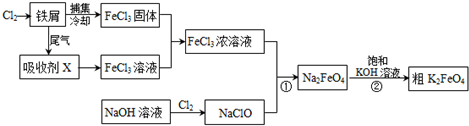
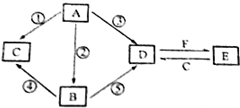 A、B、C、D、E五种物质所含元素均有两种相同,且焰色反应均为黄色,B比A相对更稳定,C、D是工业上重要的化工原料,也是实验室常用的药品,C、D在一定的条件下可以相互转化,F与A、B、C、D在一定条件下均可发生反应,它们的部分转化关系如图(部分反应物或生成物省略).
A、B、C、D、E五种物质所含元素均有两种相同,且焰色反应均为黄色,B比A相对更稳定,C、D是工业上重要的化工原料,也是实验室常用的药品,C、D在一定的条件下可以相互转化,F与A、B、C、D在一定条件下均可发生反应,它们的部分转化关系如图(部分反应物或生成物省略). ,C的俗名为火碱或烧碱;
,C的俗名为火碱或烧碱;