题目内容
【题目】下列判断正确的是( )
A.若NaA、NaB溶液的pH分别为9和8,则酸性一定是HA<HB
B.FeCl3溶液蒸干得FeCl3固体,Na2CO3溶液蒸干得Na2CO3固体
C.中和pH和体积均相同的盐酸和醋酸溶液,后者消耗NaOH的物质的量多
D.因Fe2++2H2O![]() Fe(OH)2+2H+,为抑制水解,配制Fe(NO3)2溶液时需将Fe(NO3)2溶解在稀HNO3中
Fe(OH)2+2H+,为抑制水解,配制Fe(NO3)2溶液时需将Fe(NO3)2溶解在稀HNO3中
【答案】C
【解析】
A项、没有给出NaA、NaB溶液的浓度,所以不能根据NaA、NaB溶液的pH大小判断HA和HB的酸性强弱,故A错误;
B项、FeCl3在溶液中水解生成Fe(OH)3和HCl,加热HCl挥发,促进水解平衡正移,导致FeCl3溶液蒸干得Fe(OH)3固体,碳酸钠在溶液中水解生成碳酸氢钠和氢氧化钠,碳酸氢钠和氢氧化钠都是难挥发物质,蒸发时,二者浓度变大又重新生成Na2CO3,所以蒸干得到的仍是碳酸钠固体,故B错误;
C项、pH相同的盐酸和醋酸溶液中氢离子浓度相同,由于醋酸是弱酸,部分电离,所以醋酸的浓度大,而且盐酸和醋酸的体积也相同,所以醋酸的物质的量多,所以醋酸中和的氢氧化钠多,故C正确;
D项、硝酸具有强氧化性,配制Fe(NO3)2溶液时将Fe(NO3)2溶解在稀HNO3中,亚铁离子被氧化为铁离子,故D错误;
故选C。

【题目】25℃时,三种酸的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
回答下列问题:
(1)一般情况下,当温度升高时,Ka________(填“增大”、“减小”或“不变”)。
(2)下列四种离子结合质子能力由大到小的顺序是______________________(填字母)。
a.CO32- b.ClO- c.CH3COO- d.HCO3-
(3)下列反应不能发生的是________(填字母)。
a. CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O b. ClO-+CH3COOH=CH3COO-+HClO
c. CO32-+2HClO=CO2↑+H2O+2ClO- d. 2ClO-+CO2+H2O=CO32-+2HClO
(4)25℃时,若测得CH3COOH与CH3COONa的混合溶液的pH=6,则溶液中c(CH3COO-)-c(Na+)=___mol·L-1(填精确数值)。
(5)体积均为10 mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如下图所示。
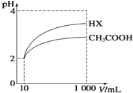
稀释后,HX溶液中水电离出来的c(H+)_____ (填“>”、“=”或“<”,下同)醋酸溶液中水电离出来的c(H+);用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸____HX。