题目内容
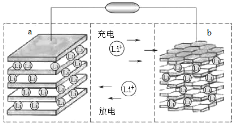
【题目】亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用氯酸钠(NaClO3)为原料制取,(常温下ClO2为气态),下列说法错误的是
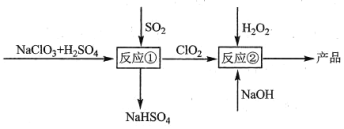
A.反应①阶段,参加反应的NaClO3和SO2的物质的量之比为2:1
B.反应①后生成的气体要净化后进入反应②装置
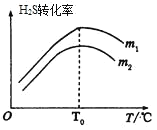
C.升高温度,有利于反应②提高产率
D.反应②中有气体生成
【答案】C
【解析】
A. 根据氧化还原反应原理,反应①阶段,NaClO3化合价降低1个价态,SO2化合价升高2个价态,根据升降守恒,则反应的NaClO3和SO2的物质的量之比为2:1,A项正确;
B. 反应物中有SO2,不处理干净,会在下一步与H2O2和NaOH反应引入杂质,B项正确;
C. 当H2O2和NaOH足量时,理论上可完全消耗ClO2,产率与温度无关,温度只会影响反应速率,C项错误;
D. 反应②条件下,ClO2化合价降低得到NaClO2,作氧化剂,H2O2化合价升高,作还原剂得到氧气,故有气体生成,D项正确;
答案选C。

 阅读快车系列答案
阅读快车系列答案【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
实验编号 | HA物质的量浓度(molL-1) | NaOH物质的量浓度(molL-1) | 混合溶液的pH |
甲 | 0.2 | 0.2 | pH=a |
乙 | c | 0.2 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,用a来说明HA是强酸还是弱酸___。
(2)不考虑其它组的实验结果,单从乙组情况分析,c是否一定等于0.2___(选填“是”或“否”).混合液中离子浓度c(A-)与c(Na+)的大小关系是___。
(3)丙组实验结果分析,HA是___酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是___。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=___molL-1。写出该混合溶液中下列算式的精确结果(不能做近似计算)
c(Na+)-c(A-)=__molL-1
c(OH-)-c(HA)=__molL-1