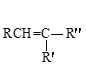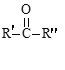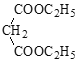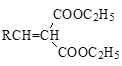题目内容
【题目】主族元素碳、氧、氮、氟、磷、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题:
(1)在基态14C原子中,核外存在___对自旋相反的电子,基态氮原子的价层电子排布图为____。
(2)将F2通入稀NaOH溶液中可生成OF2,OF2分子构型为__其中氧原子的杂化方式为_______。
(3)CuSO4溶液能用作P4中毒的解毒剂,反应可生成P的最高价含氧酸和铜,该反应的化学方程式是_____。
【答案】2 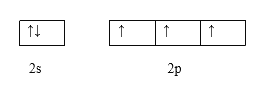 V形 sp3 P4+10CuSO4+16H2O=10Cu+4H3PO4+10H2SO4
V形 sp3 P4+10CuSO4+16H2O=10Cu+4H3PO4+10H2SO4
【解析】
(1)C原子核外电子排布式为1s22s22p2,轨道式为![]() ,氮原子的电子排布式1s22s22p3;
,氮原子的电子排布式1s22s22p3;
(2)OF2分子中O原子价层电子对数为4,孤对电子数为2;
(3)由题意可知CuSO4溶液与P4发生氧化还原反应生成铜、磷酸和硫酸。
(1)C原子核外电子排布式为1s22s22p2,轨道式为![]() ,由轨道表示式可知在基态14C原子中,核外存在2对自旋相反的电子;氮原子的电子排布式1s22s22p3,其价层电子排布图为
,由轨道表示式可知在基态14C原子中,核外存在2对自旋相反的电子;氮原子的电子排布式1s22s22p3,其价层电子排布图为![]() ,故答案为:2;
,故答案为:2;![]() ;
;
(2)OF2分子中O原子价层电子对数为4,则O原子为sp3杂化,孤对电子数为2,则其空间构型为V形,故答案为:V形;sp3;
(3)由题意可知CuSO4溶液与P4发生氧化还原反应生成铜、磷酸和硫酸,反应的化学方程式为P4+10CuSO4+16H2O=10Cu+4H3PO4+10H2SO4,故答案为:P4+10CuSO4+16H2O=10Cu+4H3PO4+10H2SO4。

 字词句段篇系列答案
字词句段篇系列答案【题目】现有下列几组物质:
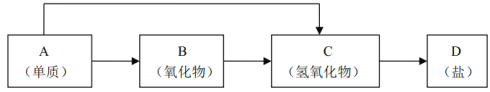
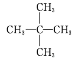
① | ② | ③ | ④ |
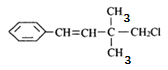
12C、14C | CH3CH3、CH3CH2CH3 | CH3CH2CH3、 |
|
(1)互为同系物的是________(填序号,下同)。
(2)互为同分异构体的是______。
(3)互为同位素的是_______。
(4)属于同一种物质的是________。