题目内容
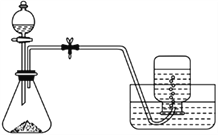
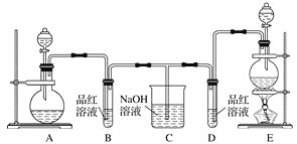
【题目】如图所示装置可进行二氧化硫的制备和某些性质的实验,请回答下列问题:

(1)A中盛放浓硫的仪器名称是______________。
(2)实验过程中,装置B试管内的___________现象证明SO2具有______性。
(3)实验过程中,装置C试管内的__________现象证明SO2具有______性,反应化学方程式为_____________。
(4)D的作用是_______。
(5)尾气可采用_____________溶液吸收。
【答案】分液漏斗 溶液由紫红色变为无色 还原性 出现黄色浑浊 氧化性 SO2+2Na2S+2H2O=3S↓+4NaOH 探究SO2与品红作用的可逆性 NaOH(氨水等)
【解析】
(1)根据装置构造判断其名称;
(2)根据二氧化硫能被酸性高锰酸钾溶液氧化分析;
(3)根据二氧化硫能把硫离子氧化为硫单质分析;
(4)根据生成的无色物质不稳定分析解答;
(5)根据二氧化硫是酸性氧化物分析。
(1)装置A中盛放浓硫的仪器名称是分液漏斗,故答案为:分液漏斗。
(2)SO2具有还原性,酸性高锰酸钾溶液具有强氧化性,和SO2发生氧化还原反应,因此实验过程中,装置B发生的现象是溶液由紫红色变为无色或紫红色酸性高锰酸钾褪色,故答案为:溶液由紫红色变为无色,还原性。
(3)SO2中S元素的化合价是+4价,具有氧化性。Na2S中S元素的化合价是-2价,具有还原性。因此SO2通入到Na2S溶液中发生氧化还原反应生成单质S沉淀,所以装置C中发生的现象是无色溶液出现黄色浑浊或,反应方程式为:SO2+2Na2S+2H2O=3S↓+4NaOH,故答案为:出现黄色浑浊,氧化性,SO2+2Na2S+2H2O=3S↓+4NaOH。
(4)二氧化硫能和有色物质反应生成无色物质,所以二氧化硫能使品红溶液褪色,但二氧化硫的漂白性不稳定,加热无色溶液时,溶液又变为红色,所以装置D的作用是探究SO2与品红作用的可逆性,故答案为:探究SO2与品红作用的可逆性。
(5)SO2是大气污染物,需要尾气处理。由于SO2是酸性氧化物,可以用氢氧化钠溶液(氨水等)吸收,故答案为:NaOH(氨水等)。