题目内容
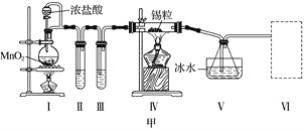
【题目】乙醛在氧化铜作催化剂的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示,试管A中装有40%的乙醛水溶液、氧化铜粉末;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下表:
物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
沸点(℃) | 20.8 | 117.9 | 290 | 197.2 | 100 |

请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为___________________________。
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在________________;目的是_______________________;当试管A内的主要反应完成后温度计水银球的位置应在__________________;目的是_____________________。
(3)烧杯B的作用是__________________,烧杯B内盛装的液体可以是__________________。(写出一种即可,在题给物质中找);某同学认为试管C最好置于冰水浴中,其目的是__________________________。
(4)对C中产品进行蒸馏时,蒸馏烧瓶中加入少量____,以除去其中含有的少量水。
A.浓硫酸 B.CaO C.CuSO4溶液 D.无水CaCl2
(5)以下区分乙酸精品和粗品的方法,合理的是_____。
A.加入水观察实验现象
B.加入足量氢氧化钠溶液后,再加入银氨溶液,水浴加热观察实验现象
C.加入碳酸氢钠溶液,振荡后观察实验现象
D.加入少量Na单质,振荡后观察实验现象
【答案】 2CH3CHO+O2![]() 2CH3COOH 试管A的反应液中 测量反应溶液的温度 试管A的支管口处 收集含乙酸的馏分 使试管A内的反应液均匀受热发生反应,使生成的乙酸变成蒸气进入试管C; 乙二醇(甘油) 有利于乙酸的冷凝收集 D B
2CH3COOH 试管A的反应液中 测量反应溶液的温度 试管A的支管口处 收集含乙酸的馏分 使试管A内的反应液均匀受热发生反应,使生成的乙酸变成蒸气进入试管C; 乙二醇(甘油) 有利于乙酸的冷凝收集 D B
【解析】(1)乙醛与氧气发生氧化反应生成乙酸,方程式为:2CH3CHO+O2![]() 2CH3COOH,故答案为:2CH3CHO+O2
2CH3COOH,故答案为:2CH3CHO+O2![]() 2CH3COOH;
2CH3COOH;
(2)实验开始时温度计应测量反应的温度,控制反应温度为60℃~80℃,所以实验开始时温度计水银球的位置应在试管A的反应液中;由蒸馏原理可知,温度计测量的是蒸气的温度,所以温度计水银球的位置应在试管A的支管口处,故答案为:试管A的反应液中;测量反应溶液的温度;试管A的支管口处;收集含乙酸的馏分;
(3)乙酸的沸点为117.9℃,要想通过蒸馏的方法得到乙酸,B内盛装的液体的沸点应大于117.9℃,由表可知烧杯B内盛装的液体可以是乙二醇或甘油,B中装的液体直接受热,可以让试管A内的反应液均匀受热发生反应,试管C最好置于冰水浴中,其目的是有利于乙酸的冷凝收集,故答案为:使试管A内的反应液均匀受热发生反应,使生成的乙酸变成蒸气进入试管C;乙二醇(甘油);有利于乙酸的冷凝收集;
(4)对C中产品进行蒸馏时,蒸馏烧瓶中装加入少量无水CaCL2,以出去其中含有的少量水。A.浓硫酸和乙酸反应,故A错误;B.CaO 吸收水分同时和乙酸反应,故B错误;C.CuSO4溶液不能吸收水分,故C错误;D.无水CaCl2吸收水分,不与乙酸反应,故D正确;故答案为:D;
(5)乙酸粗品中含乙醛,区分乙酸精品和粗品的方法是加入足量氢氧化钠溶液后,再加入银氨溶液,水浴加热观察实验现象。A.加入水观察实验现象不能区分,故A错误;B.加入足,量氢氧化钠溶液后,再加入银氨溶液,水浴加热观察实验现象,出现此现象说明为粗品,故B正确;C.二者都含有乙酸,都能和碳酸氢钠反应生成气体加入碳酸氢钠溶液,震荡后观察实验现象不能区别二者,故C错误;D.二者都含有乙酸,都能和Na单质反应放出气体,振荡后观察实验现象不能区别二者,故D错误;故答案为:B。

 全能测控期末小状元系列答案
全能测控期末小状元系列答案【题目】X、Y、Z、M、W、Q、R是7种短周期元素,其原子半径及主要化合价如下:
元素代号 | X | Y | Z | M | W | Q | R |
原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
主要化合价 | +1 | +3 | +6,﹣2 | +7,﹣1 | +5,﹣3 | ﹣2 | +1 |
完成下列填空:
(1)上述元素中,金属性最强的在周期表中的位置是________________________________;X、Y、Q各自形成的简单离子中,离子半径由大到小的顺序是_______(填离子符号)。
W和R按原子个数比1﹕4构成的阳离子所含的化学键是____________________。
(2)表中所列4种第三周期元素的最高价氧化物的水化物碱性最弱的是_______(填化学
式),其电离方程式为_____________________________________。
(3)M与Z相比,非金属性较强的是_____________(填元素名称),请从原子结构的角度说明理由_________________________________________________________________。
(4)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应,反应方程式如下:
![]() KMnO4+
KMnO4+![]() H2O2+
H2O2+![]() H2SO4 →
H2SO4 → ![]() K2SO4+
K2SO4+![]() MnSO4+
MnSO4+![]() O2↑+
O2↑+![]() H2O
H2O
请配平,当有0.5 mol H2O2参加此反应,电子转移的个数为______________________。
【题目】根据下列实验操作和现象所得出的结论错误的是
选项 | 操作 | 现象 | 结论 |
A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状炭,并放出有刺激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
B | 向盛有浓氨水的锥形瓶中通入氧气,并将灼热铂丝置于液面上方 | 铂丝保持红热,且瓶内有白烟产生 | 氨的催化氧化反应为放热反应 |
C | 向盛有H2O2溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后,溶液中出现气泡,随后有红褐色沉淀生成 | Fe2+催化H2O2分解产生O2;H2O2分解反应放热,促进Fe2+的水解平衡正向移动 |
D | 向浓度均为0.1mol/L的MgCl2和CuC12的混合溶液中逐滴加入氨水 | 先出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
A. A B. B C. C D. D