题目内容
向一定量的Fe、FeO和Fe2O3的混合物中加入120 mL 4 mol·L-1的稀硝酸,恰好使混合物完全溶解,放出1.344 L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热条件下还原相同质量的混合物,能得到铁的物质的量为( )
| A.0.24 mol | B.0.21 mol | C.0.16 mol | D.0.14 mol |
B
依据题意可知参加反应的HNO3(0.48 mol)分成两部分,一部分生成NO(0.06 mol),另一部分生成Fe(NO3)2,依据N原子守恒可知Fe(NO3)2中的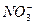 物质的量为0.48 mol-0.06 mol=0.42 mol,所以Fe(NO3)2物质的量为
物质的量为0.48 mol-0.06 mol=0.42 mol,所以Fe(NO3)2物质的量为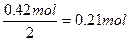 ,即混合物中含铁的物质的量为0.21 mol。
,即混合物中含铁的物质的量为0.21 mol。
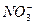 物质的量为0.48 mol-0.06 mol=0.42 mol,所以Fe(NO3)2物质的量为
物质的量为0.48 mol-0.06 mol=0.42 mol,所以Fe(NO3)2物质的量为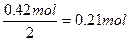 ,即混合物中含铁的物质的量为0.21 mol。
,即混合物中含铁的物质的量为0.21 mol。
练习册系列答案
 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
 Cu2S+3SO2+2FeO(炉渣);
Cu2S+3SO2+2FeO(炉渣);