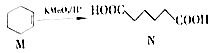题目内容
【题目】某待测溶液中只可能含有Ag+、Fe2+、Na+、Ba2+、 ![]() 、
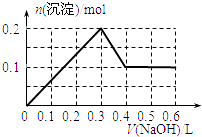
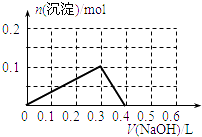
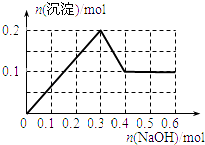
、 ![]() 、
、 ![]() 中的几种离子,依次进行下列实验: ①取少量待测液,加入足量的NaCl溶液,没有明显现象
中的几种离子,依次进行下列实验: ①取少量待测液,加入足量的NaCl溶液,没有明显现象
②继续加入足量的Na2SO4溶液,有白色沉淀生成
③过滤,取少量滤液,加入足量的NaOH溶液,有白色絮状沉淀生成,迅速变为灰绿色,最后变为红褐色
根据实验现象回答:
(1)待测液中一定含有离子,一定没有离子.
(2)写出步骤②中发生反应的离子方程式 .
(3)写出步骤③中沉淀由白色变为红褐色的化学方程式 .
【答案】
(1)Fe2+、Ba2+、NO3﹣; Ag+、CO32﹣、SO42﹣
(2)SO42﹣+Ba2+=BaSO4↓
(3)4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】解:(1)由以上分析可知,溶液中一定存在的离子为Fe2+、Ba2+、NO3﹣,一定不存在的离子为Ag+、CO32﹣、SO42﹣,
故答案为:Fe2+、Ba2+、NO3﹣;Ag+、CO32﹣、SO42﹣;(2)步骤②中发生反应的反应为硫酸根离子与钡离子反应生成硫酸钡,反应的离子方程式为SO42﹣+Ba2+=BaSO4↓;
故答案为:SO42﹣+Ba2+=BaSO4↓;(3)步骤③中沉淀由白色变为红褐色,是氢氧化亚铁与氧气反应生成氢氧化铁的反应,反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
由①取少量待测液,加入足量的NaCl溶液,无明显现象,溶液中一定不存在Ag+;
②继续加入足量的Na2SO4溶液,有白色沉淀生成,溶液中一定存在Ba2+,则一定不存在SO42﹣和CO32﹣,根据溶液电中性可知,溶液中一定存在唯一的阴离子NO3﹣;
③过滤,取少量滤液,加入足量NaOH溶液,有白色絮状沉淀生成,迅速变成灰绿色,最终变成红褐色,该现象说明溶液中一定存在Fe2+,以此来解答.

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案