��Ŀ����
11���Թ�ҵ�ϳɰ�������̽��һֱ�ǻ�ѧ��ҵ����Ҫ���⣬�ں��º��ݵļ����������º�ѹ���������зֱ���кϳɰ���Ӧ����ͼ��ͼ����ʾ���ݾ�Ϊ��ʼ����������t���Ӻ�Ӧ���ﵽƽ�⣬���ɵ�NH3��Ϊ0.4mol������ˮ��ѹǿ��Ӱ�켰�������ܽ⣩��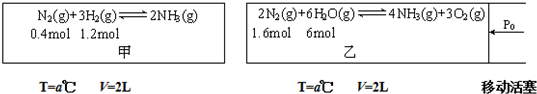
���жϼ������еķ�Ӧ��ƽ���������ACE������д��Ӧ��ţ�
A��ѹǿ����ʱ��ı� B��������ܶȲ���ʱ��ı� C��c��N2������ʱ��ı�
D����λʱ��������2mol NH3��ͬʱ����1mol N2
E����λʱ���ڶ���3mol H-H����ͬʱ����6mol N-H��
�ڸ������¼������з�Ӧ��ƽ�ⳣ��K=$\frac{400}{27}$��ƽ��ʱ����ѹǿPƽ=$\frac{3}{4}$P0
���ó�ʼѹǿP0��ʾ����
���� �ٿ��淴Ӧ����ƽ��ʱ��ͬ�����ʵ�����������ȣ�����ֵ�Ũ�ȡ��������ֲ��䣬�ɴ�����������һЩ�����䣬�ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����仯˵������ƽ�⣻
�ڼ�����t���Ӻ�Ӧ���ﵽƽ�⣬���ɵ�NH3��Ϊ0.4mol����
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol����0.4 1.2 0
�仯����mol����0.2 0.6 0.4
ƽ������mol����0.2 0.6 0.4
�ٸ���K=$\frac{{c}^{2}��N{H}_{3}��}{c��{N}_{2}����{c}^{3}��{H}_{2}��}$����ƽ�ⳣ�������º�����ѹǿ֮�ȵ����������ʵ���֮�ȣ�
��� �⣺��A���淴Ӧ�����������ʵ�����С�����º�����������ѹǿ��С����ѹǿ����ʱ��ı䣬˵������ƽ��״̬����A��ȷ��
B������������������䣬�����ݻ����䣬���������ܶ�Ϊ��ֵ����B����
C������ƽ��ʱ�����Ũ�ȱ��ֲ��䣬c��N2������ʱ��ı䣬˵���ﻯѧƽ��״̬����C��ȷ��
D����λʱ��������2molNH3��ͬʱ����1molN2������ʾ����Ӧ���ʣ���Ӧʼ�հ��ñ�����ϵ���У���D����
E����λʱ���ڶ���3molH-H����ͬʱ����6molN-H����������6molN-H��������3molH-H������������������������������ȣ���Ӧ����ƽ�⣬��E��ȷ��
��ѡ��ACE��
�ڼ�����t���Ӻ�Ӧ���ﵽƽ�⣬���ɵ�NH3��Ϊ0.4mol����
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol����0.4 1.2 0
�仯����mol����0.2 0.6 0.4
ƽ������mol����0.2 0.6 0.4
��ƽ�ⳣ��K=$\frac{{c}^{2}��N{H}_{3}��}{c��{N}_{2}����{c}^{3}��{H}_{2}��}$=$\frac{��\frac{0.4}{2}��^{2}}{\frac{0.2}{2}����\frac{0.6}{2}��^{3}}$=$\frac{400}{27}$��
���º�����ѹǿ֮�ȵ����������ʵ���֮�ȣ���ƽ��ʱ����ѹǿPƽ=$\frac{1.2mol}{1.6mol}$P0=$\frac{3}{4}$P0��
�ʴ�Ϊ��$\frac{400}{27}$��$\frac{3}{4}$P0��
���� ���⿼�黯ѧƽ����㡢ƽ��״̬�жϣ�ע������ʽ�ڻ�ѧƽ�������Ӧ�ã�ע���ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����ٱ仯˵������ƽ�⣮

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д���֪��

����˵����ȷ���ǣ�������
| A�� | H2��I2��HI�����еĻ�ѧ�����ǷǼ��Թ��ۼ� | |
| B�� | �Ͽ�2 mol HI�����еĻ�ѧ����������ԼΪ��c+b+a��kJ | |
| C�� | ��ͬ�����£�1molH2��g����1mol I2��g��������С��2mol HI��g���������� | |
| D�� | ���ܱ������м���2mol H2��g����2mol I2��g������ַ�Ӧ��ų�������Ϊ2akJ |
��1��I-��HCO3-��NO3-��OH-
��2��K+��Mg2+��CO32-��Cl-
��3��Mg2+��SO42-��Cl-��HCO3-
��4��Al3+��Cu2+��SO42-��Cl-
��5��H+��K+��AlO2-��HSO3-
��6��Pb2+��Na+��SO42-��NO3-��
| A�� | ��1���ͣ�6�� | B�� | ��3���ͣ�4�� | C�� | ��2���ͣ�4�� | D�� | ��2���ͣ�5�� |
| A�� | ƽ���ƶ���Kֵһ���仯 | B�� | Kֵ�仯��ƽ��һ���ƶ� | ||
| C�� | ƽ���ƶ���Kֵ���ܲ��� | D�� | Kֵ���䣬ƽ������ƶ� |
| Ԫ�� | �����Ϣ |
| M | ����������Ӧ��ˮ�����ܰ�1��1�������������ȵ����������� |
| Q | ��������������������������֮��Ϊ4���ǽ�������ͬ����Ԫ������ǿ |
| X | �䵥��Ϊ����ɫ���� |
| Y | ij�ֺ���ԭ�ӵ�������Ϊ56��������Ϊ30 |
| Z | XԪ�صĵ�����ZԪ�صĵ�����ȼ�գ���������������ɫ���� |
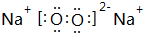
��3��M��Q��Z�����ӵİ뾶�ɴ�С��˳��ΪCl-��O2-��Na+�������ӷ��ű�ʾ��
��4����һ����ѧ����ʽ��ʾ֤���ǽ�����Q��X��H2S+Cl2=2HCl+S��
��5��5.6L��״���µ�X�ļ��⻯����������Z��������ȫȼ������Һ̬ˮʱ���ų�������Ϊ356.8kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ2H2S��g��+3O2��g��=2SO2��g��+2H2O��l����H=-2854.4kJ/mol
��6���ڼ��������£�Q�ĵ��ʿ���YZ2-��Ӧ�Ʊ�һ�ֿ����ھ�ˮ����YZ42-���÷�Ӧ�����ӷ���ʽΪ3Cl2+2FeO2-+8OH-=2FeO42-+6Cl-+4H2O��
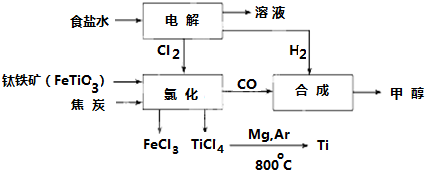
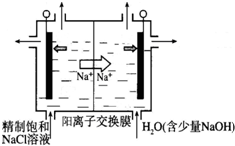 �������ȣ�ClO2��Ϊһ�ֻ���ɫ���壬�ǹ����Ϲ��ϵĸ�Ч�����ס����١���ȫ��ɱ����������
�������ȣ�ClO2��Ϊһ�ֻ���ɫ���壬�ǹ����Ϲ��ϵĸ�Ч�����ס����١���ȫ��ɱ����������