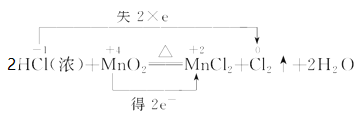
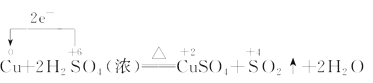题目内容
【题目】下列叙述中正确的是
A. CS2为V形的极性分子,形成分子晶体
B. ClO3-的空间构型为平面三角形
C. 氯化硼BCl3的熔点为-107 ℃,氯化硼液态时能导电而固态时不导电
D. SiF4和SO32-的中心原子均为sp3杂化,SiF4分子呈空间正四面体,SO32-呈三角锥形
【答案】D
【解析】
A. CS2和CO2相似,为直线形分子,在固态时形成分子晶体,故A不选;
B. ClO3-的中心原子的价层电子对数为![]() ,其VSEPR模型为正四面体,略去中心原子上的孤电子对,ClO3-的空间构型为三角锥形,故B不选;
,其VSEPR模型为正四面体,略去中心原子上的孤电子对,ClO3-的空间构型为三角锥形,故B不选;
C. 氯化硼BCl3的熔点为-107 ℃,氯化硼为分子晶体,液态和固态时只存在分子,没有离子,所以不能导电,故C不选;
D. SiF4和SO32-的中心原子的价层电子对数均为4,所以中心原子均为sp3杂化,SiF4的中心原子为sp3杂化,没有孤电子对,所以分子呈空间正四面体,SO32-有一对孤电子对,所以分子呈三角锥形,故D选。
故选D。

 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案【题目】根据表中信息判断,下列选项不正确的是( )
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | MnO | Cl2、Mn2+ |
A. 第①组反应的其余产物为H2O和O2
B. 第②组反应中参加反应的Cl2与FeBr2的物质的量之比为1∶2
C. 第③组反应中生成1 mol Cl2,转移电子 2 mol
D. 氧化性由强到弱顺序为MnO![]() >Cl2>Fe3+>Br2
>Cl2>Fe3+>Br2
【题目】某无色溶液甲中仅含有下列离子的几种( 不考虑水的电离以及离子的水解);
阳离子 | K+、Al3+、Fe3+、Ba2+、NH4+ |
阴离子 | Cl-、CO32-、HCO3-、SO42- |
取100mL溶液甲并分成两等份进行如下实验(假设每步完全反应):
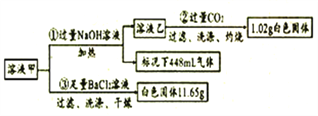
(1)由①可知,原溶液存在的离子有____,浓度为_____mol/L。
(2)写出实验②中生成沉淀的离子方程式_________。
(3)通入过量CO2充分反应后,需将反应后的混合溶液加热再过滤,其目的是_______。
(4)某同学通过分析认为该溶液中一定存在K+,其理由是________。