题目内容
把足量的铁粉投入到稀盐酸和氯化铜的混合溶液中,充分反应后,残余固体的质量与原来加入的铁粉质量相等,则原溶液中H+和Cl-的物质的量之比为( )
| A.1∶4 | B.1∶7 | C.1∶8 | D.2∶5 |
C
设氯化氢和氯化铜的物质的量分别是x和y。则根据方程式Fe+2HCl=FeCl2+H2↑、Fe+CuCl2=FeCl2+Cu可知,(0.5x+y)×56=64y,解得y=3.5x。所以原溶液中H+和Cl-的物质的量之比为x︰(x+2y)=1∶8,答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
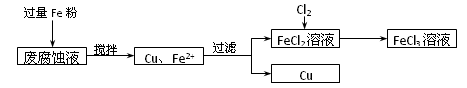

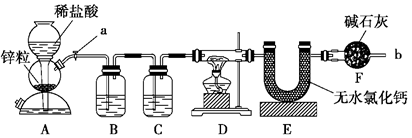
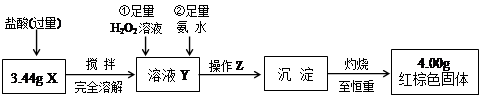

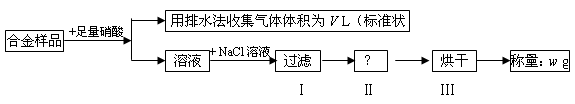
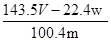 ×100%
×100%