��Ŀ����
����Ŀ�������£���Ũ��Ϊ0.1 mol��L��1�����ΪV L�İ�ˮ����μ���һ��Ũ�ȵ����ᣬ��pH�Ʋ���Һ��pH������ļ����������͵ĵζ����ߣ�d��������Һǡ����ȫ��Ӧ������ͼ����Ϣ�ش��������⣺

(1)���¶�ʱNH3��H2O�ĵ��볣��K��________��
(2)����������������pH��________��
(3)�Ƚ�b��c��d����ʱ����Һ�У���ˮ�������c(OH��)��С˳��Ϊ___________��(����ĸ)
(4)�ζ�ʱ����b�㵽c��Ĺ����У����и�ѡ������ֵ������___(����ĸ����ͬ)��
A��c(H��)��c(OH��) B. c(H��)��c(NH3��H2O)/c(NH4+)
C. c(NH4+)��c(OH��)/c(NH3��H2O) D. c(H��)/c(OH��)
(5)�������ϵζ������ж�����˵����ȷ����________(��Һ��NԪ��ֻ����NH4+��NH3��H2O������ʽ)��
A����b��ʾ��Һ�У�c(NH4+)��c(H��)��c(OH��)��c(NH3��H2O)
B����c��ʾ��Һ�У�c(Cl��)��c(NH3��H2O)��c(NH4+)
C����d��ʾ��Һ�У�c(Cl��)>c(H��)>c(NH4+)>c(OH��)
D���ζ������п����У�c(NH3��H2O)>c(NH4+)>c(OH��)>c(Cl��)>c(H��)
(6)d��֮������������������ͼ���е�e��(������NH4+ˮ���Ӱ��)����e���Ӧ�ĺ�����Ϊ________��
���𰸡�10��5 1 d >c > b D D 11V/9
��������
�����£���Ũ��Ϊ0.1 mol��L��1�����ΪV L�İ�ˮ����μ���һ��Ũ�ȵ����ᣬ���߷�Ӧ�����Ȼ�泥���Һ��pH��С��ǡ�÷�Ӧʱ笠�ˮ����Һ�����ԣ������μ�����ʱ��������������������ˮ�ĵ��룬���ͼ�������������
��1���ζ�ǰ��ˮ��������Ũ����10��11mol/L�������ˮ�����ӻ�������֪��Һ����������Ũ����0.001mol/L������¶�ʱNH3��H2O�ĵ��볣��K��![]() ��
��
��2����ͼ���֪dʱ�������������백ˮ�������ͬ������ǡ�÷�Ӧ������NH3��H2O��HCl��֪�ζ����������������Ũ����0.1mol/L������������Һ��pH��1��
��3����b��ʱ������Ϊһˮ�ϰ����Ȼ�泥�һˮ�ϰ��ĵ���̶ȴ����Ȼ�淋�ˮ��̶ȣ���Һ�Լ��ԣ���ˮ�ĵ������������á���c��ʱ������Ϊһˮ�ϰ����Ȼ�泥�һˮ�ϰ��ĵ���̶ȵ����Ȼ�淋�ˮ��̶ȣ���Һ�����ԣ���ˮ�ĵ���ƽ��û��Ӱ�졣��d��ʱ����Ϊ�Ȼ�泥�笠�ˮ�������ԣ���ˮ�ĵ�����ٽ����ã�����b��c��d����ʱ����Һ�У���ˮ�������c(OH��)��С˳��Ϊd��c��b��
��4���ζ�ʱ����b�㵽c��Ĺ����У����и�ѡ������ֵ������___(����ĸ����ͬ)��
A���¶Ȳ��䣬ˮ�����ӻ��������䣬����c(H��)��c(OH��)���䣻
B. �¶Ȳ��䣬����ƽ�ⳣ����ˮ�����ӻ��������䣬c(H��)��c(NH3��H2O)/c(NH4+)��c(H��)��c(NH3��H2O)��c(OH��)/c(NH4+)��c(OH��)��KW/Kb���¶Ȳ��䣬�ñ�ֵ���䣻
C. c(NH4+)��c(OH��)/c(NH3��H2O)��Kb���¶Ȳ��䣬����ƽ�ⳣ�����䣻
D. �ζ�ʱ����b�㵽c��Ĺ����У�������Ũ�Ȳ����������������ӵ�Ũ�Ȳ��ϼ�С�����c(H��)/c(OH��)�ı�ֵ����
��ѡD��
��5��A����ͼ���֪��b��Ӧ����Һ���Ȼ����һˮ�ϰ����ʵ���֮��Ϊ1��1�Ļ�����Һ�Լ��ԣ�˵��һˮ�ϰ��ĵ���̶ȴ���笠���ˮ��̶ȣ��ɵ���غ�c(NH4+)��c(H��)��c(OH��)��c(Cl��)�������غ�2c(Cl��)��c(NH3��H2O)��c(NH4+)��֪��ʾ��Һ�У�c(NH4+)��2c(H��)��2c(OH��)��c(NH3��H2O)��A����
B����ͼ���֪��c��ʾ��Һ��pH��7����c(H��)��c(OH��)���ɵ���غ�c(NH4+)��c(H��)��c(OH��)��c(Cl��)��֪c(Cl��)��c(NH4+)�������Һ��c(Cl��)��c(NH3��H2O)��c(NH4+)��B����
C����ͼ���֪dʱ�������������백ˮ�������ͬ������ǡ�÷�Ӧ�����Ȼ�泥�笠�ˮ����Һ�����ԣ����d��ʾ��Һ�У�c(Cl��)��c(NH4+)��c(H��)��c(OH��)��C����
D����һˮ�ϰ��϶࣬�����HCl����ʱ�����Ȼ����������Һ�а�ˮŨ��Զ�����Ȼ��Ũ�ȣ���˵ζ������п����У�c(NH3��H2O)��c(NH4+)��c(OH��)��c(Cl��)��c(H��)��D��ȷ��
��ѡD��
��6������������ΪxL��e��ʱ��Һ��pH��2����0.1mol/L��xL��0.1mol/L��VL��0.01mol/L����

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
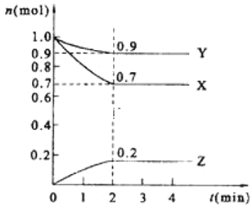
Сѧ��10����Ӧ����ϵ�д�����Ŀ��t��ʱ�������������ܱ������з�����Ӧ:X(g)+3Y(g)![]() 2Z(g)��������ڲ�ͬʱ�̵�Ũ�����������˵����ȷ����( )
2Z(g)��������ڲ�ͬʱ�̵�Ũ�����������˵����ȷ����( )
���� | X | Y | Z |
��ʼŨ��/mol/L | 0.1 | 0.2 | 0 |
2minĩŨ��/mol/L | 0.08 | a | b |
ƽ��Ũ��/mol/L | 0.05 | 0.05 | 0.1 |
A. ƽ��ʱ��X��ת����Ϊ20% B. t��ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ40
C. ����ƽ������ϵѹǿ��v������v���С��ƽ��������Ӧ�����ƶ� D. ǰ2min�ڣ���Y�ı仯���ʾ��ƽ����Ӧ����v(Y)=0.03mol/(L��min)
����Ŀ��ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯����100mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų�����������ʵ���¼�����Ϊ�ۼ�ֵ���ѻ���ɱ�״������
ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
���������mL�� | 50 | 120 | 232 | 290 | 310 |
��1����һʱ��Σ�ָ0��1��1��2��2��3��3��4��4��5 min����Ӧ�������___��ԭ����___��
��2����һ��ʱ�εķ�Ӧ������С___��ԭ����___��
��3����2��3����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ���ʣ�����Һ������䣩___��
��4�������Ӧ̫���ң�Ϊ�˼�����Ӧ���ʶ��ֲ����ٲ����������������������зֱ����������������Һ��
A������ˮ B��NaCl��Һ C��NaNO3��ҺD��Na2CO3��Һ
����Ϊ���е��ǣ����ţ�___��