题目内容
将等质量的两份足量的锌粉a、b分别加入到等量的稀硫酸,同时向a中加少量CuSO4溶液,下图中产生H2的体积V(L)与时间t(min)的关系,其中正确的是( )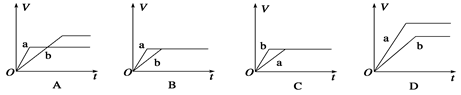
B
解析试题分析:由于锌足量,稀硫酸等量,故产生气体物质的量相等,即体积相等。a中加入硫酸铜溶液,反应速率加快,先完成放映。故选择B选项。
考点:化学反应速率图像

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在密闭容器中进行下列反应M(g)+N(g) R(g)+2L:反应符合如图所示的图象.下列叙述正确的是
R(g)+2L:反应符合如图所示的图象.下列叙述正确的是
| A.正反应吸热,L是气体 |
| B.正反应吸热,L是固体 |
| C.正反应放热,L是气体 |
| D.正反应放热,L是固体或液体 |
下列事实不能用勒夏特列原理解释的是
| A.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| B.H2、I2、HI混合气体加压后颜色变深 |
| C.红棕色的NO2加压后颜色先变深再变浅 |
| D.工业上生产硫酸的过程中使用过量的空气,以提高二氧化硫的利用率 |
下列变化过程中,ΔS<0的是
| A.氯化钠溶于水中 | B.NH3(g)和HCl(g)反应生成NH4Cl |
| C.干冰的升华 | D.CaCO3(S)分解为CaO(S)和CO2(g) |
在密闭容器中,反应X2(g)+Y2(g) 2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是( )
2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是( )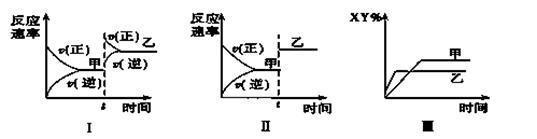
| A.图Ⅰ是增大压强的变化情况 |
| B.图Ⅱ是一定是加入催化剂的变化情况 |
| C.图Ⅲ是增大压强或升高温度的变化情况 |
| D.图Ⅲ一定是升高温度的变化情况 |
化学平衡常数K的数值大小是衡量化学反应进行程度的标志,在常温下,下列反应的平衡常数的数值如下:2NO(g) N2(g)+O2(g) K1=1×1030
N2(g)+O2(g) K1=1×1030
2H2(g)+O2(g) 2H2O(g) K2=2×1081
2H2O(g) K2=2×1081
2CO2(g) 2CO(g)+O2(g) K3=4×10-92
2CO(g)+O2(g) K3=4×10-92
以下说法正确的是 ( )
| A.常温下,NO分解产生O2的反应的平衡常数表达式为K1=c(N2)·c(O2) |
| B.常温下,水分解产生O2,此时平衡常数的数值约为5×10-80 |
| C.常温下,NO、H2O、CO2三种化合物分解放出O2的倾向由大到小的顺序为NO>H2O>CO2 |
| D.以上说法都不正确 |
今有X(g)+Y(g)  2Z(g) △H<0。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,引起t2→t3曲线变化的原因是
2Z(g) △H<0。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,引起t2→t3曲线变化的原因是
| A.增大X或Y的浓度 | B.增大压强 |
| C.增大Z的浓度 | D.升高温度 |
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) nY(g) ΔH=QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示,下列说法正确的是
nY(g) ΔH=QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示,下列说法正确的是
| 容器体积/L c(Y)/mol/L 温度/℃ | 1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
A.m>n B.温度不变,压强增大,Y的质量分数减少
C.Q<0 D.体积不变,温度升高,平衡向逆反应方向移动
在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g)
|
B.A、B、C的浓度相等
C.单位时间生成 n mol A,同时生成 3n mol B
D.生成C的速率与C分解的速率相等
