题目内容
11.下列变化中,吸收的热量用于克服分子间作用力的是( )| A. | 加热金属铝使之融化 | B. | 液氨受热蒸发 | ||
| C. | 加热碘化氢气体使之分解 | D. | 加热硅晶体使之融化 |
分析 分子晶体的构成微粒是分子,只有分子晶体发生物理变化时破坏分子间作用力,金属晶体熔融需要克服金属键、离子晶体发生熔融时克服离子键、原子晶体熔融时克服共价键,据此分析解答.
解答 解:A.金属铝构成微粒是金属阳离子和自由电子,铝中存在金属键,熔融时需要破坏金属键,故A不选;
B.液氨属于分子晶体,受热蒸发时只发生物理变化,需要破坏分子间作用力,故B选;
C.加热HI分解需要破坏化学键,故C不选;
D.硅属于原子晶体,熔融时需要破坏共价键,故D不选;
故选B.
点评 本题考查化学键和分子间作用力的区别,分子晶体只发生物理变化时破坏分子间作用力,但发生化学反应时破坏化学键,易错选项是D.

练习册系列答案
相关题目
1.下列烃中,一卤代物的同分异构体的数目最少和最多的分别是( )
| A. | 乙烷 | B. | 2-甲基丙烷 | C. | 2,2-二甲基丙烷 | D. | 2,2-二甲基丁烷 |
2.A、B是短周期元素,两元素能形成B2A型离子化合物,B离子比A离子少一个电子层,已知A的原子序数为n,则B的原子序数为( )
| A. | n-5 | B. | n+3 | C. | n+13 | D. | n-13 |
19.某强酸性溶液X中含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验内容如下:

根据以上信息,下列观点正确的是( )

根据以上信息,下列观点正确的是( )
| A. | 沉淀G的化学式为Fe(OH)2 | |
| B. | 生成气体A的离子方程式为2Fe2++NO3-+4H+=2Fe3++NO↑+2H2O | |
| C. | 反应②中的离子方程式有AlO2-+CO2+2H2O=Al(OH)3+HCO3- | |
| D. | 溶液X中,除H+ 外还肯定含有的离子是NH4+、Fe2+、SO42-. |
6.下列结论错误的是( )
①微粒半径:r(K+)>r(Al3+)>r(S2-)>r(Cl-)
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>H2SiO3
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
①微粒半径:r(K+)>r(Al3+)>r(S2-)>r(Cl-)
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>H2SiO3
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
| A. | ① | B. | ①③ | C. | ②③④⑤⑥⑦ | D. | ①③⑤ |
3.某有机物结构如图所示,则下列关于该有机物的说法中不正确的是( )
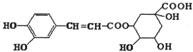
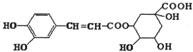
| A. | 该有机物在一定条件下可以发生消去反应 | |
| B. | 1mol该有机物与足量的溴水反应时最多消耗4molBr2 | |
| C. | 该有机物不能使酸性高锰酸钾溶液褪色 | |
| D. | 该有机物在一定条件下可以发生水解反应和酯化反应 |
20.下列各组物质不属于同分异构体的是( )
| A. | 乙醇与甲醚 | B. | 麦芽糖与纤维二糖 | ||
| C. | 淀粉与纤维素 | D. | 2-甲基丁烷和戊烷 |
1.下列各有机物的命名正确的是( )
| A. | 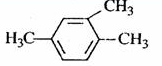 1,3,4-三甲苯 | B. | 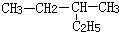 2-乙基丁烷 2-乙基丁烷 | ||
| C. | 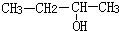 3-丁醇 3-丁醇 | D. | 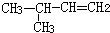 3-甲基-1-丁烯 3-甲基-1-丁烯 |
 氮、硫、氯及其化合物是中学化学重要的组成部分.
氮、硫、氯及其化合物是中学化学重要的组成部分.