题目内容
【题目】(1)比较结合H+能力的相对强弱:H2O_____NH3(填“>”、“<”或“=”);用一个离子方程式说明H3O+和NH4+给出H+能力的相对强弱_____。
(2)NaCN是离子化合物,各原子均满足8电子稳定结构。写出NaCN的电子式_____。
(3)乙酸汽化时,测定气体的相对分子质量,有数据表明其摩尔质量变为120g·mol-1,从结构上分析其可能的原因是______。
【答案】< H3O++NH3=NH4++H2O ![]() 两个气态乙酸分子通过氢键结合
两个气态乙酸分子通过氢键结合
【解析】
(1)H3O+又能够与氨气反应生成NH4+,据此判断;
(2)NaCN是离子化合物,各原子均满足8电子稳定结构,据此书写电子式;
(3)乙酸的相对分子质量为60,据此分析解答。
(1)H3O+能够与氨气反应生成NH4+,因此结合H+能力的相对强弱:H2O<NH3,反应的方程式为:H3O++NH3=NH4++H2O;
(2)NaCN是离子化合物,各原子均满足8电子稳定结构,根据C.N的原子最外层的电子数,结合形成8电子稳定结构需要的共用电子对数目可知,NaCN的电子式为![]() ;
;
(3)乙酸汽化时,测定气体的相对分子质量,有数据表明其摩尔质量变为120gmol1,乙酸的相对分子质量为60,说明是两个气态乙酸分子通过氢键结合形成蒸气分子。

【题目】已知SiO2+2C![]() Si+2CO↑;Si+C
Si+2CO↑;Si+C![]() SiC。
SiC。
现有石英砂和炭粉的混合物1mol,于高温下在电炉里充分反应后,得残留固体;若石英砂与混和物的物质的量之比n(0<n<1),试讨论n取何值时,残留物的成分及其物质的量。
n | 例︰n= | __ | __ | __ | __ |
残留固体及物质的量(摩) | Si | __ | __ | __ | __ |
___________。
【题目】用如图所示装置制取表中的四种干燥、纯净的气体![]() 图中加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂。上述方法中可以得到干燥、纯净的气体是( )
图中加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂。上述方法中可以得到干燥、纯净的气体是( )
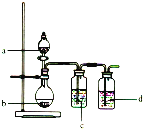
气体 | a | b | c | d |
| 稀盐酸 |
| 饱和 | 浓 |
| 浓盐酸 |
| NaOH溶液 | 浓 |
| 稀 | Cu | 品红溶液浓 |
|
| 稀盐酸 | 锌粒 | NaOH溶液 | 浓 |
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()