题目内容
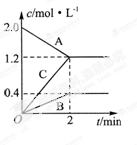
下图是可逆反应X2+3Y2 2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是
2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是
| A.t1时,只有正方向反应 | B.t1~t2时,X2的物质的量越来越多 |
| C.t2~t3,反应不再发生 | D.t2~t3,各物质的浓度不再发生变化 |
D
解析试题分析:从图象中知:横坐标表示时间、纵坐标表示反应速率.该反应开始时只有X2 (g)、Y2 (g)。
A、0~t1,向正反应方向进行,反应物的浓度不断减少,V正不断减小,同时有了产物Z2(g),V逆由0逐渐增大,V正>V逆,故A错误;B、t2时,V正==V逆≠0,反应达到平衡状态,所以t1~t2时,X2的物质的量越来越少,故B错误;C、t2时,V正==V逆≠0,反应达到平衡状态,但反应未停止,各浓度不变,故C错误;D、t2~t3,V正==V逆≠0,反应达到平衡状态,各物质的浓度不再发生变化,故D正确,答案选D。
考点:考查可逆反应平衡状态的判断
点评:该题是中等难度的试题,试题基础性强,主要是考查学生对可逆反应平衡状态的建立、平衡状态的特征等有关知识的了解掌握情况,意在培养学生分析、归纳和总结问题的能力,有利于调动学生的学习兴趣,激发学生的学习积极性。抓住化学平衡的标志,来判断反应是否已达平衡.根据平衡的特点解题,是该题求解的关键。

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)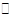 4NO2 +O2(g)△H>0,T1温度下的部分实验数据为:
4NO2 +O2(g)△H>0,T1温度下的部分实验数据为:
| t/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)mol/L | 5.00 | 3.55 | 2.50 | 2.50 |
下列说法中,正确的是:
A.当反应体系内气体的平均相对分子质量不再发生变化时则该反应达到了平衡
B.T1温度下的平衡常数为K1=125,500s时N2O5的转化率为71%:
C.其他条件不变时,T2温度下反应到2000s时测得N2O5 (g)浓度为2.78mol/L, 则T1<T2
D.T1温度下的平衡常数为K1,若维持T1温度不变,增加体系压强,达到新的平衡时,平衡常数为K2,则K2>K1
在25℃时,密闭容器中X、Y、Z三种气体的浓度变化情况如图: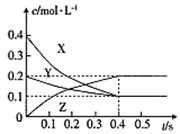
下列说法错误的是( )
A.反应可表示为3X+Y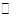 2Z 2Z |
| B.从反应开始到0.4s时,以Y表示的化学反应速率为:0.25mol·L-1·s-1 |
| C.增大压强使平衡向生成Z的方向移动,平衡常数增大 |
| D.升高温度,平衡常数可能增大也可能减小 |
工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2 2SO3,这是一个放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中,错误的是
2SO3,这是一个放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中,错误的是
| A.使用催化剂是为了加快反应速率,提高生产效率 |
| B.在上述条件下,SO2不可能100%地转化为SO3 |
| C.达到平衡时,改变反应条件可能在一定程度上改变该反应的化学平衡状态 |
| D.达到平衡时,SO2的浓度与SO3的浓度一定相等 |
将H2(g)和Br2(g)充入恒容密闭容器中,恒温下发生反应H2(g)+Br2(g)  2HBr(g) (正反应放热),平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。 a与b的关系是
2HBr(g) (正反应放热),平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。 a与b的关系是
| A.a>b | B.a =b | C.a <b | D.无法确定 |
为探究足量锌与稀硫酸的反应速率(以v(H2)表示),向反应混合液中加入某些物质,下列判断正确的是( )
| A.加入NH4HSO4固体,v(H2)不变,生成H2量不变 |
| B.加入少量水,v(H2)减小,生成H2量减少 |
| C.加入CH3COONa固体,v(H2)减小,生成H2量不变 |
| D.滴加少量CuSO4溶液,v(H2)增大,生成H2量减少 |

 3C (g) 。下列叙述中表明该可逆反应一定达到平衡状态的是
3C (g) 。下列叙述中表明该可逆反应一定达到平衡状态的是