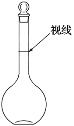
题目内容
【题目】
已知:①A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
(1)A的化学名称为_______。
(2)B的结构简式为______,其核磁共振氢谱显示为______组峰,峰面积比为______。
(3)C中官能团的名称为:_______。
(4)由C生成D的化学方程式:___________________________________。
(5)由C生成E的化学方程式:___________________________________。
(6)已知F是A的同系物,F的相对分子质量比A多28,则与F互为同分异构体且能发生银镜反应的结构种类有_____________种。
【答案】 丙酮 ![]() 2 1:6 碳碳双键、氰基
2 1:6 碳碳双键、氰基 
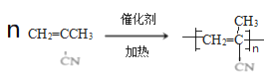 4种
4种
【解析】试题分析:A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰,A的分子式是C3H6O,结构简式是CH3COCH3;CH3COCH3与HCN发生加成反应生成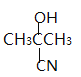 ,
,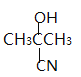 在浓硫酸作用下发生消去反应生成
在浓硫酸作用下发生消去反应生成![]() ,
,![]() 与氯气在光照条件下发生取代反应生成
与氯气在光照条件下发生取代反应生成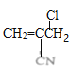 ;
;![]() 在一定条件下发生加聚反应生成高聚物E,E是
在一定条件下发生加聚反应生成高聚物E,E是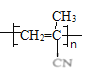 。
。
解析:根据以上分析,(1)A是CH3COCH3,化学名称为丙酮。
(2)丙酮与HCN发生加成反应生成B,B是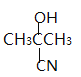 ,结构简式为
,结构简式为![]() ,其核磁共振氢谱显示为2组峰,峰面积比为1:6。
,其核磁共振氢谱显示为2组峰,峰面积比为1:6。
(3)![]() 中官能团的名称为:碳碳双键、氰基。
中官能团的名称为:碳碳双键、氰基。
(4)![]() 与氯气在光照条件下发生取代反应生成
与氯气在光照条件下发生取代反应生成 的化学方程式:
的化学方程式: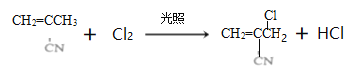 。
。
(5)![]() 在一定条件下发生加聚反应生成高聚物
在一定条件下发生加聚反应生成高聚物 的化学方程式是:
的化学方程式是: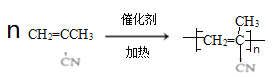 。
。
(6)F的相对分子质量比A多28,则F的分子式是C5H10O,能发生银镜反应说明含有醛基,则F的结构有CH3CH2CH2CH2CHO、CH3CH2CH(CH3)CHO、(CH3)2CHCH2CHO、(CH3)3CCHO 共4种。

【题目】三氯化六氨合钴(Ⅲ)是一种重要的配合物原料,实验室制备实验流程如下:
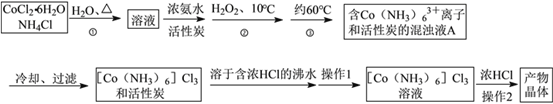
已知:[Co(NH3)6]Cl3在水中电离为[Co(NH3)6]3+和Cl-,[Co(NH3)6]Cl3的溶解度如下表:
温度(℃) | 0 | 20 | 47 |
溶解度(g) | 4.26 | 6.96 | 12.74 |
(1)第①步需在煮沸NH4Cl溶液中加入研细的CoCl2·6H2O晶体,加热煮沸与研细的目的是__
(2)实验室制备三氯化六氨合钴(III)的化学方程式为:____________
(3)实验操作1为 _________[Co(NH3)6]Cl3溶液中加入浓盐酸的目的是_____
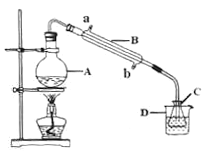
(4)现称取0.2675g[Co(NH3)6]Cl3(相对分子质量为267.5),在A中发生如下反应:[Co(NH3)6]Cl3+3NaOH![]() Co(OH)3↓+6NH3↑+3NaCl(装置见右下图),C中装0.5000mol·L-1的盐酸25.00mL,D中装有冰水。加热烧瓶,使NH3完全逸出后,用少量蒸馏水冲洗导管下端外壁上粘附的酸液于C中,加入2-3滴甲基红指示剂,用0.5000mol·L-1的NaOH滴定。
Co(OH)3↓+6NH3↑+3NaCl(装置见右下图),C中装0.5000mol·L-1的盐酸25.00mL,D中装有冰水。加热烧瓶,使NH3完全逸出后,用少量蒸馏水冲洗导管下端外壁上粘附的酸液于C中,加入2-3滴甲基红指示剂,用0.5000mol·L-1的NaOH滴定。
已知: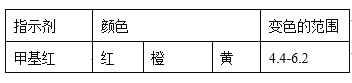
①当滴定到终点时,共需消耗NaOH溶液___mL(准确到0.01mL)。
②当用上述原理测定某[Co(NH3)x]Cl3晶体中x值,实验过程中未用少量蒸馏水冲洗导管下端内外壁上粘附的酸液于C中,则x值将______(填“偏大”、“偏小”或“不变”)
【题目】应用 VSEPR 理论判断下表中分子或离子的立体构型。
分子 | 中心原子上弧电子对数 | 中心原子结合的杂化类型 | 分子或离子的立体构型 |
NH2 | _______________ | _______________ | _______________ |
BF3 | _______________ | _______________ | _______________ |
H3O+ | _______________ | _______________ | _______________ |