题目内容
【题目】下面是s能级与p能级的原子轨道图:
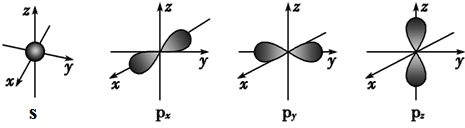
请回答下列问题:
(1)s电子的原子轨道呈_____形,每个s能级有_____个原子轨道;
(2)p电子的原子轨道呈_____形,每个p能级有_____个原子轨道.
(3)Na、Mg、Al第一电离能的由大到小的顺序:__________________。
(4)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列:①2s ②3d ③4s ④3s ⑤4p ⑥3p轨道能量由低到高排列顺序是_______。
【答案】球 1 哑铃或纺锤 3 Mg>Al>Na ①④⑥③②⑤
【解析】
s电子的原子轨道呈球形,p电子的原子轨道呈哑铃形或纺锤形,s、p、d、f能级的原子轨道数分别为1、3、5、7;同周期第一种元素的第一电离能最小,最后一种元素的第一电离能(稀有气体)最大,同族元素从上到下第一电离能变小;绝大多数基态原子核外电子的排布都遵循下列顺序(能量由低到高):1s、2s、2p、3s、3p、4s、3d、4p、5s、4d、5p、6s、4f、5d、6p、7s…。
(1)s电子的原子轨道呈球形,每个s能级只有1个原子轨道;
(2)p电子的原子轨道呈哑铃形或纺锤形,每个p能级有3个原子轨道;
(3)Na、Mg、Al分别位于第三周期ⅠA族、ⅡA族、ⅢA族,根据每周期第一种元素的第一电离能最小,最后一种元素的第一电离能(稀有气体)最大,所以第一电离能的由大到小的顺序为:Mg>Al>Na;
(4) 绝大多数基态原子核外电子的排布都遵循下列顺序(能量由低到高):1s、2s、2p、3s、3p、4s、3d、4p、5s、4d、5p、6s、4f、5d、6p、7s…,所以题目中轨道能量由低到高排列顺序为:①④⑥③②⑤。

 考前必练系列答案
考前必练系列答案【题目】利用如图所示装置测定中和热的实验步骤如下:
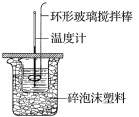
①用量筒量取50mL0.50mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50mL0.55mol·L-1NaOH溶液,并用同一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:
(1)使盐酸与NaOH溶液混合均匀的正确操作是___(填字母)。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(2)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L1mol·L-1的稀盐酸恰好完全反应,其反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3的大小关系为___。
(3)假设盐酸和氢氧化钠溶液的密度都是1g·cm-3,又知中和反应后生成溶液的比热容c=4.18J·g-1·℃-1。为了计算中和热,某学生实验记录数据如下:
实验序号 | 起始温度t1/ ℃ | 终止温度t2/ ℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=___(结果保留一位小数)。
(4)____(填“能”或“不能”)用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是__。
【题目】某小组探究清洗试管(内壁附着银镜)的反应原理,进行下列实验。
I.初步探究
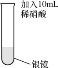
(1)将稀硝酸加入附着银镜的试管中,记录现象如下:
实验Ⅰ | 实验操作 | 实验现象 |
| 银镜上出现气泡,在液面下方为无色气体,在试管口附近......;试管内壁上的银逐渐溶解。 |
①补全反应中的实验现象___。
②实验Ⅰ中银镜消失发生反应的化学方程式为____。
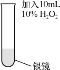
(2)为消除实验Ⅰ中氮氧化物的污染,将双氧水溶液加入附着银镜的试管中。
实验Ⅱ | 实验操作 | 实验现象 |
| 剧烈反应,有大量无色气体产生,该气体可以使带火星的木条复燃;试管内壁上的银逐渐溶解。 |
①由现象推测H2O2将Ag氧化为Ag+,但通过实验排除了这种可能。该实验方案是:在反应后的液体中,加入___。
②查阅资料发现:该实验中银镜溶解后最终产物为颗粒很小(直径在1~100nm之间)的Ag,其分散在液体中,肉眼无法识别。该同学通过实验证实了这种可能性。他的操作及现象是:___。
③写出该实验Ⅱ中发生反应的化学方程式:___。
II.查阅资料,继续探究
查阅文献:Ag2O+4NH3H2O=2[Ag(NH3)2]++2OH-+3H2O
(3)探究Ag2O在H2O2分解反应中的作用,进行如下实验。
实验Ⅲ | 实验操作 | 实验现象 |
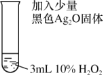
| 剧烈反应,产生大量的无色气体,同时在试管底部仍有少量黑色固体 |
根据实验Ⅲ的现象猜想:Ag2O在反应中作氧化剂。继续实验,在实验Ⅲ反应后的试管中加入足量的溶液x后,固体仍有剩余。由此验证了该猜想的正确。
①在实验中加入足量的溶液x是____。
②实验Ⅲ中发生反应的化学方程式为___。