题目内容
【题目】常温下,0.2molL﹣1的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法不正确的是( ) 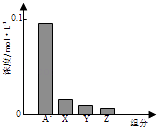
A.HA为弱酸
B.该混合液pH>7
C.图中X表示HA,Y表示OH﹣ , Z表示H+
D.该混合溶液中:c(A﹣)+c(Y)=c(Na+)
【答案】C
【解析】解:一元酸HA和NaOH溶液等体积、等浓度0.2mol/L混合,HA+NaOH=NaA+H2O,所得溶液中A﹣浓度小于0.1mol/L,说明在溶液中存在A﹣+H2OHA+OH﹣ , NaA水解,HA为弱酸,NaA溶液呈碱性,则c(OH﹣)>c(H+),一般来说,盐类的水解程度较低,则有c(A﹣)>c(OH﹣),所以有:c(Na+)=0.1mol/L>c(A﹣)>c(OH﹣)>c(HA)>c(H+),即X表示OH﹣ , Y表示HA,Z表示H+ , 溶液中存在物料守恒得到:c(Na+)=c(A﹣)+c(HA). A.一元酸HA和NaOH溶液等体积、等浓度0.2mol/L混合,二者恰好反应:HA+NaOH=NaA+H2O,所得溶液为NaA溶液,溶液中中A﹣浓度小于0.1mol/L,说明在溶液中存在A﹣+H2OHA+OH﹣ , NaA水解,HA为弱酸,故A正确;
B.c(Na+)>c(A﹣),说明NaA水解,A﹣+H2OHA+OH﹣ , 该混合液pH>7,故B正确;
C.HA是弱电解质,则有c(A﹣)>c(OH﹣),c(OH﹣)除了水解产生的还有水电离的,因此c(OH﹣)>c(HA),所以有:c(Na+)=0.1mol/L>c(A﹣)>c(OH﹣)>c(HA)>c(H+),即X表示OH﹣ , Y表示HA,Z表示H+ , 故C错误;
D.溶液中存在物料守恒c(Na+)=c(A﹣)+c(HA),Y表示HA,得到c(A﹣)+c(Y)=c(Na+),故D正确;
故选C.
一元酸HA和NaOH溶液等体积、等浓度0.2mol/L混合,HA+NaOH=NaA+H2O,所得溶液中A﹣浓度小于0.1mol/L,说明在溶液中存在A﹣+H2OHA+OH﹣ , NaA水解,HA为弱酸,NaA溶液呈碱性,则c(OH﹣)>c(H+),一般来说,盐类的水解程度较低,则有c(A﹣)>c(OH﹣),所以有:c(Na+)=0.1mol/L>c(A﹣)>c(OH﹣)>c(HA)>c(H+),即X表示OH﹣ , Y表示HA,Z表示H+ , 溶液中存在物料守恒为:c(Na+)=c(A﹣)+c(HA).

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案