题目内容
【题目】(1)写出浓硫酸与木炭粉在加热条件下反应的化学方程式_____________ ;
(2)用如图所示装置可检验木炭和浓硫酸反应产生的混合气体中含有SO2和CO2。
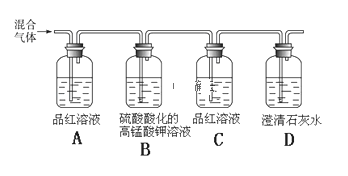
①能够证明混合气体中含有SO2的实验现象是:________________________________;
②设计B、C的实验目的是:________________________________________________;
③写出B中发生反应的离子方程式:_____________________________;
④能够证明混合气体中含有CO2的实验现象是:_____________________。
【答案】2H2SO4(浓)+C![]() CO2↑+SO2↑+2H2O A中品红溶液褪色 除去SO2并检验SO2,气体是否除尽,排除SO2对CO2气体检验的干扰 5SO2+2MnO4﹣+2H2O=5SO42﹣+2Mn2++4H+ C中品红溶液不褪色D中溶液变浑浊
CO2↑+SO2↑+2H2O A中品红溶液褪色 除去SO2并检验SO2,气体是否除尽,排除SO2对CO2气体检验的干扰 5SO2+2MnO4﹣+2H2O=5SO42﹣+2Mn2++4H+ C中品红溶液不褪色D中溶液变浑浊
【解析】
根据碳和硫酸反应生成二氧化硫、二氧化碳和水分析,二氧化硫能使品红褪色,但二氧化碳不能,二氧化碳能使澄清石灰水反应变浑浊,二氧化硫也能,故先检验二氧化硫并除去,后检验二氧化碳。
(1)碳和浓硫酸反应生成二氧化硫和二氧化碳和水,方程式为2H2SO4(浓)+C![]() CO2↑+SO2↑+2H2O;
CO2↑+SO2↑+2H2O;
(2)①二氧化硫能使品红褪色,故A中品红溶液褪色;
②因为二氧化硫也能使澄清石灰水变浑浊,故先除去SO2并检验SO2气体是否除尽,排除SO2对CO2气体检验的干扰;
③二氧化硫能被高锰酸钾氧化,离子方程式为:5SO2+2MnO4﹣+2H2O=5SO42﹣+2Mn2++4H+;
④二氧化硫完全除去后才能根据澄清石灰水的现象分析,故能够证明混合气体中含有CO2的实验现象是:C中品红溶液不褪色D中溶液变浑浊。