题目内容
【题目】某实验研究小组欲检验草酸晶体分解的产物并测定草酸溶液的浓度(杂质不发生反应)。查阅资料:草酸晶体(H2C2O4·2H2O)在100 ℃开始失水,101.5 ℃熔化,150 ℃左右分解产生H2O、CO和CO2。下面是可供选择的实验仪器(图中某些加热、夹持装置已略去),实验所需药品不限。
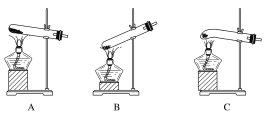
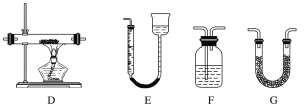
(1)最适宜加热分解草酸晶体的装置是C。若选装置A可能会造成的后果是______________;若选装置B可能会造成的后果是_________________________________。
(2)实验利用装置“G(碱石灰)—F—D(CuO固体)—F”检验CO,则F中盛装的试剂是_______,证明含有CO的现象是_____________________________________________。
(3)可用0.10 mol/L酸性KMnO4标准溶液来滴定未知浓度的草酸溶液。
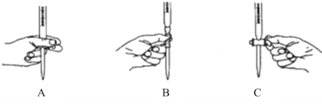
①滴定过程中发生反成的离子方程式为_________________________________________。②滴定过程中操作滴定管的图示正确的是_________。
③判断反应达到滴定终点时的现象为__________________________________________。
【答案】固体药品熔化后会流到试管口,不利于草酸晶体分解 冷凝水会倒流到试管底,造成试管炸裂 澄清的石灰水 前一个F中没有浑浊现象出现,D中固体颜色由黑色变为红色,后一个F中有浑浊现象出现 2MnO4-+ 5H2C2O4 + 6H+= 2Mn2++ 10CO2↑+ 8H2O A 当滴入最后一滴标准液时,溶液由无色变为紫红色且30s不褪色
【解析】
(1)草酸晶体的熔点低,受热容易熔化,用C装置加热分解革酸晶体,熔融的固体不易流下,适用于加热草酸,若选择装置A加热会使固体熔融物溶化后流到试管口处,若选择装置B分解生成的水会倒流试管底部炸裂试管;
(2)实验利用装置“G(碱石灰)-F-D(CuO固体)-F”检验CO,通过装置G吸收水和二氧化碳,通过装置F检验二氧化碳是否除净,通过装置D检验是否有一氧化碳含有氧化铜为铜,最后通过装置F检验是否生成二氧化碳气体;
(3)①高锰酸钾具有强氧化性,把草酸中的C从+3价氧化成+4价的二氧化碳,Mn元素从+7价变化到+2价的锰离子,由于草酸分子中有2个C原子,所以高锰酸钾与草酸的反应比例为5:2,故反应的方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
②根据滴定管的使用规则,滴定时,左手包住滴定管的活塞控制液滴的滴出,防止活塞被意外打开;
③可利用高锰酸钾溶液自身的颜色作为指示剂判断滴定终点。
(1)最适宜加热分解革酸晶体的装置是C,若选装置A可能会造成的后果是固体药品熔化后会流到试管口,不利于草酸晶体分解;若选装置B可能会造成的后果是冷凝水会倒流到试管底,造成试管破裂,
故答案为:固体药品熔化后会流到试管口,不利于草酸晶体分解;冷凝水会倒流到试管底,造成试管破裂。
(2)实验利用装置“G(碱石灰)-F-D(CuO固体)-F”检验CO,通过装置G吸收水和二氧化碳,通过装置F检验二氧化碳是否除净,通过装置D检验是否有一氧化碳含有氧化铜为铜,最后通过装置F检验是否生成二氧化碳气体,
故答案为:澄清的石灰水;前一个F中没有浑浊现象出现,D中固体颜色由黑色变为红色,后一个F中有浑浊现象出现。
(3)①高锰酸钾具有强氧化性,把草酸中的C从+3价氧化成+4价的二氧化碳,Mn元素从+7价变化到+2价的锰离子,由于草酸分子中有2个C原子,所以高锰酸钾与草酸的反应比例为 5:2,故反应的方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,
故答案为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。
②根据滴定管的使用规则,滴定时,左手包住滴定管的活塞控制液滴的滴出,防止活塞被意外打开,即如图A所示操作,故答案为:A。
③可利用高锰酸钾溶液自身的颜色作为指示剂判断滴定终点,当滴入最后一滴标准液时,溶液由无色变为紫红色且30s不褪色,故答案为:当滴入最后一滴标准液时,溶液由无色变为紫红色且30s不褪色。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】某实验小组用 0.50 mol/L NaOH 溶液和 0.50 mol/L 硫酸溶液在如下图所示的装置中 进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
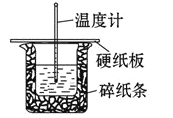
(1)从实验装置上看,图中缺少的一种玻璃仪器是_____。
(2)烧杯间填满碎纸条的作用是_____。
(3)若大烧杯上不盖硬纸板,求得的反应热数值______填“偏大”“偏小”或“无影响”)。
(4)若取取 50 mL NaOH 溶液和 30 mL 硫酸溶液进行实验,实验数据如下表。
温度 实验次数 | 起始温度 t1/℃ | 终止温度t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 30.1 |
2 | 27.0 | 27.4 | 27.2 | 33.3 |
3 | 25.9 | 25.9 | 25.9 | 29.8 |
4 | 26.4 | 26.2 | 26.3 | 30.4 |
近似认为 0.50 mol/L NaOH 溶液和 0.50 mol/L 硫酸溶液的密度都是 1 g/cm3,中和后生成溶液 的比热容 c=4.18 J/(g·℃)。则中和热△H=_____(取小数点后一位)。