题目内容
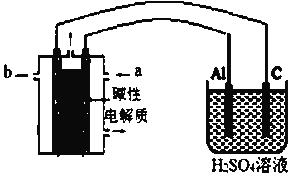
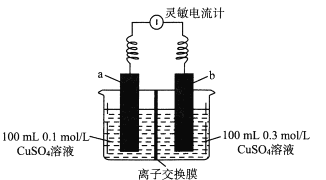
【题目】按如图装置进行实验(a、b电极均为Cu电极),实验开始观察到灵敏电流计的指针发生偏转。 下列有关说法正确的是
A. b极电极反应为Cu - 2e-=Cu2+B. 溶液中Cu2+穿过交换膜发生迁移
C. 电流计指针偏转幅度将保持不变D. 外电路转移的电子最多为0.02 mol
【答案】D
【解析】
灵敏电流计指针发生偏转,说明有电流产生,则装置一定是原电池,负极电极反应式是Cu-2e-=Cu2+,正极反应不可能发生2H++2e-=H2↑,因此正极反应必是Cu2++2e-=Cu,溶液中离子从高浓度的右室经过离子交换膜迁往低浓度的左室才是自发过程,如果溶液中迁移Cu2+,由于负极与正极消耗或产生的Cu2+相等,则左、右两室溶液浓度不变,但负极Cu减少,正极Cu增加,需要消耗能量而不可能提供电能,所以溶液中迁移离子不可能是Cu2+,就只能是SO42-,从右室向左室迁移,因此b为正极,a为负极;
A、该装置浓度差电池,浓度增大,还原性或氧化性增强,右侧CuSO4浓度大,氧化性增强,因此b电极为正极,a电极为负极,电极反应式为Cu-2e-=Cu2+,故A错误;
B、溶液中离子从高浓度的右室经过离子交换膜迁往低浓度的左室才是自发过程,如果溶液中迁移Cu2+,由于负极与正极消耗或产生的Cu2+相等,则左、右两室溶液浓度不变,但负极Cu减少,正极Cu增加,需要消耗能量而不可能提供电能,所以溶液中迁移离子不可能是Cu2+,就只能是SO42-,从右室向左室迁移,故B错误;
C、随着电流的产生,左、右两室SO42-浓度的差值逐渐减小,SO42-从右室向左室迁移的速率逐渐减小,则外电路的电流强度将逐渐减小,灵敏电流计指针偏转的幅度也会逐渐减小,故C错误;
D、当左右两室SO42-浓度相等,即均为(0.3mol·L-1+0.1mol·L-1)/2时,电池将停止工作,不再有电流产生,溶液中迁移的n(SO42-)=0.1L×[0.3mol·L-1-(0.3mol·L-1+0.1mol·L-1)/2]=0.01mol,因此外电路转移电子物质的量最多为0.02mol,故D正确。

【题目】某小组同学探究物质的溶解度大小与沉淀转化方向之间的关系。已知:
物质 | BaSO4 | BaCO3 | AgI | AgCl | |
溶解度/g(20℃) | 2.4×10-4 | 1.4×10-3 | 3.0×10-7 | 1.5×10-4 |
(1)探究BaCO3和BaSO4之间的转化
实验操作: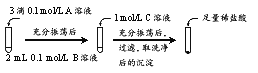
试剂A | 试剂B | 试剂C | 加入盐酸后的现象 | |
实验Ⅰ | BaCl2 | Na2CO3 | Na2SO4 | …… |
实验Ⅱ | Na2SO4 | Na2CO3 | 有少量气泡产生,沉淀部分溶解 |
① 实验Ⅰ说明BaCO3全部转化为BaSO4,依据的现象是加入盐酸后,______。
② 实验Ⅱ中加入稀盐酸后发生反应的离子方程式是______。
③ 实验Ⅱ说明沉淀发生了部分转化,结合BaSO4的沉淀溶解平衡解释原因:______。
(2)探究AgCl和AgI之间的转化
实验Ⅲ: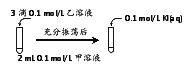
实验Ⅳ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:a>c>b>0)。
装置 | 步骤 | 电压表读数 | |
| ⅰ.如图连接装置并加入试剂,闭合K | a | |
ⅱ.向B中滴入AgNO3(aq),至沉淀完全 | b | ||
ⅲ.再向B中投入一定量NaCl (s) | c | ||
ⅳ.重复ⅰ,再向B中加入与ⅲ等量NaCl(s) | a |
注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
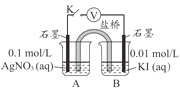
① 实验Ⅲ证明了AgCl转化为AgI,甲溶液可以是______(填序号)。
a. AgNO3溶液 b. NaCl溶液 c. KI溶液
② 实验Ⅳ的步骤ⅰ中,B中石墨上的电极反应式是______。
③ 结合信息,解释实验Ⅳ中b<a的原因:______。
④ 实验Ⅳ的现象能说明AgI转化为AgCl,理由是______。
(3)综合实验Ⅰ~Ⅳ,可得出结论: ______。