��Ŀ����
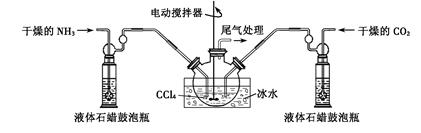
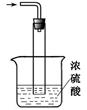
ijУ̽��ѧϰС��ͬѧ�ú�����������(��ҪΪ������ɳ��CaCl2��MgCl2��Na2SO4��)�Ĵ�����ȡ����ѧ��������NaCl��ʵ��ǰ������������·���(��ͼ)�� 
(1)��д�������ڢܡ��ݲ������Լ����Ƽ��ڢ��������ƣ��� ���� ���� ��
(2) ���������C�Ļ�ѧ�ɷ���(�����ֺͻ�ѧʽ��ʾ)�� ��
(3)д���ڢݲ������п��ܷ�����Ӧ�����ӷ���ʽ��
��
(4)��������������ڢݲ�ʵ���Ƿ�ﵽ��Ŀ�ģ�
��
(5)����Ϊ���������Щ���������Ӱ��ʵ������ ��
(6)��ͬѧ��Ϊ����ʵ����Ʋ�����Լ����������һ�����룺
��
�Ţ�̼������Һ ������ �������������ᾧҲ�ɣ�����1�֣�
�� ��ɳ��BaSO4��BaCO3��CaCO3��Mg(OH)2��2�֣�
�ǵڢݲ���H+ + OH- = H2O ��1�֣� CO32- + 2H+ = H2O + CO2����1�֣�
�� �ò�����պȡ��Һ����pH��ֽ�в�������죬˵����Һ�����ԣ���OH-��CO32-���ڣ���������˵����Һ�Գʼ��ԣ���OH-��CO32-���ڣ�������μ������������ԡ���2�֣�
�ɢں͢ۻ�ۺ͢ܣ�2�֣�
�� ��Ba (OH)2����BaCl2��NaOH��ʹ�ڢ۲��ϲ�Ϊһ����1�֣�
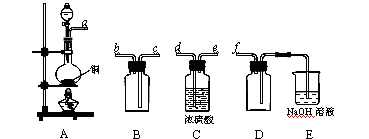
���������������1����������ͼ�Ѹ������Լ������ã�BaCl2��Һ��ȥNa2SO4��NaOH��Һ��ȥMgCl2�����Ԣܵ�����Ϊ��ȥCaCl2����ѡ�Լ�ΪNa2CO3��Һ���ݵ������dz�ȥ������NaOH��Na2CO3��Ӧѡ�����ᣬ�������Ǵ�NaCl��Һ�еõ���ѧ��NaCl��Ϊ����������
��2��BaCl2��NaOH��Na2CO3��Ӧ��õ��ij������У���ɳ��BaSO4��BaCO3��CaCO3��Mg(OH)2��
��3���ڢݲ�����HCl����NaOH��Na2CO3��Ӧ���������ӷ���ʽΪ��H+ + OH- = H2O�� CO32- + 2H+ = H2O + CO2����
��4��HCl����ʱ�ڢݲ��ﵽ��Ŀ�ģ�����pH��ֽ���飬����ֽ�仯��֤��HCl������OH?��CO32?�����ڣ���������˵������OH?��CO32?��������μ������������ԡ�
��5��NaOH��Ӱ���������ʵij�ȥ������NaOH�ļ���˳�������ǰ��Ҳ���������������ں͢ۻ�ۺܿ͢ɵ�����
��6����Ba (OH)2����BaCl2��NaOH����ͬʱ��ȥNa2SO4��MgCl2��ʹ�ڢ۲��ϲ�Ϊһ����
���㣺���⿼������ͼ�ķ������Լ���ѡ�������������ӷ���ʽ����д��ʵ�鷽������ƺͷ�����

ʵ������ȡ���ᶡ����ʵ��װ�������¼ס�������װ�ÿɹ�ѡ�á�

���ף� ���ң�
�Ʊ����ᶡ�����漰���й����ʵ��������ʼ��±�
| | ���� | 1������ | ���ᶡ�� |
| �۵�(��) | 16��6 | ��89��5 | ��73��5 |
| �е�(��) | 117��9 | 117 | 126��3 |
| �ܶ�(g/cm3) | 1��05 | 0��81 | 0��88 |
| ˮ���� | ���� | ���� (9g/100gˮ) | �� |
��1����ȡ���ᶡ����װ��Ӧѡ��___________(��ס����ҡ�)����ѡ��һ��װ�õ�������______________________________________________________________��
��2����ʵ���������г������������ᶡ���⣬���������ɵ��л��������У�д���ṹ��ʽ��________________________________________________________________��
��3��������Ӧ��һ�����淴Ӧ��Ϊ���1�������������ʣ�д�����ֿ��еķ�����
�� ����
��4�����Ʊ����ᶡ�����õĻ�����з��롢�ᴿ���ᶡ��ʱ����Ҫ�����ಽ����������ͼʾ�IJ����У��϶���Ҫ�Ļ�ѧ������________________��ѡ��𰸱�ţ���





A B C D
��5���л���ķ�������У�������Ҫʹ�÷�Һ©����������ʹ�÷�Һ©��ǰ����_______________��ijͬѧ�ڽ��з�Һ����ʱ��������Һ�����������������ԭ�����Һ©�����������⣬���� ��
̼�����׳ƴ������;�ܹ㡣ʵ�����У���̼����狀ͱ���ʳ��ˮ���Ƶô���������ڲ�ͬ�¶��µ��ܽ�ȼ�����
  �¶ȡ� �¶ȡ��ܽ�� ���� g/100gˮ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| NH4HCO3 | 15.8 | 21.0 | 27.0 | | | | |
| NaHCO3 | 8.2 | 9.6 | 11.1 | 12.7 | 14.4 | 16.4 | |
| NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 |
ʵ�鲽��
�����뾫�ƣ��ٴ���(��Ca2+��Mg2+��SO42��)�ܽ⣻�ڼ�������NaOH��Na2CO3��Һ����У��۹��ˣ��ܼ��������pH��7��
��ת�����ٽ����ƺ��ʳ����Һ�¶ȿ�����30~35��֮�䣻�ڲ��Ͻ����£�������ϸ��̼����泥����£������Сʱ���ھ��ã� a �� b ���۵õ�NaHCO3���塣
���ƴ�����õ�NaHCO3�����������У��ھƾ��������գ���ȴ�����£����õ����
���������գ�
��1���������뾫�ơ��ɳ�ȥ�Ĵ����е����������� ��
��2����ת���������ӷ���ʽ�� ��
��3����ת���������У��¶ȿ�����30~35��֮��ļ��ȷ�ʽ�� ��Ϊʲô�¶ȿ�����30~35��֮�䣿 ��
��4��a��b���IJ����ֱ��� �� ��
��5��ʵ�����ƵõĴ������NaCl�����ܺ�����NaHCO3��Ϊ�ⶨ����Ĵ��ȣ��õ�����ƽȷ��ȡ��ƷG�ˣ����������ƿ������������ˮ�ܽ⣬�μ�2�η�̪����c mol/L�ı�����ζ�����Һ��dz��ɫ�����ɫ�Ұ���Ӳ��䣬�ζ������������������������������ΪV1 mL����ʱ�����ķ�ӦΪ��CO32�� + H+ ��HCO3��
����Ʒ��̼���������ٷֺ����ı���ʽ�� ��
������ƿ��Һ�м����μ�2�μ��ȣ���ͬŨ�ȵ���������ζ����յ㣬������������ΪV2mL���ζ��յ�ʱ��Һ��ɫ�ı仯�� ������ʵ�����ݣ�����ж���Ʒ����NaHCO3 ��
�������ȣ�ClO2����Ŀǰ�����Ϲ��ϵĵ��Ĵ���Ч�����Ĺ�������������һ�ֻ���ɫ�����壬������ˮ��ʵ���ҿ���NH4Cl�����ᡢNaClO2���������ƣ�Ϊԭ�����Ʊ�ClO2�����������£�
��1��д�����ʱ������Ӧ�Ļ�ѧ����ʽ�� ��
��2����ȥClO2�е�NH3��ѡ�õ��Լ��� ��������ĸ��
| A������ʳ��ˮ | B����ʯ�� | C��Ũ���� | D��ˮ |
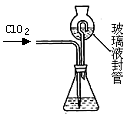
��װ���в���Һ��ܵ������� �� ��
����д��������������������⻯����Һ��Ӧ�����ӷ���ʽ �� ��
�۵ζ��յ�������ǣ� ��
�ܲ��ͨ��ClO2������m(ClO2)= �����ú�c��V�Ĵ���ʽ��ʾ������֪��ClO2����Է�������Ϊ67.5��
��4�����ʵ����ȷ����ҺX�ijɷ֣��벹�����ʵ�鲽�������
| ʵ�鲽�� | ʵ������ | ʵ����� |
| �� | | ��ҺX�к���Na+ |
| �� | | ��ҺX�к���Cl�� |



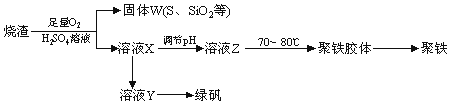





 NH2COONH4(s) + Q (Q > 0 )
NH2COONH4(s) + Q (Q > 0 )