题目内容
12.常温下,下列物质的溶液pH>7的是( )| A. | K2SO4 | B. | NH4Cl | C. | Na2CO3 | D. | Cu(NO3)2 |
分析 常温下,溶液的pH>7,说明该溶液呈碱性,溶液中的溶质可能是碱或强碱弱酸盐,据此分析解答.
解答 解:常温下,溶液的pH>7,说明该溶液呈碱性,溶液中的溶质可能是碱或强碱弱酸盐,
A.K2SO4是强碱强酸盐,其溶液呈中性,故A错误;
B.NH4Cl是强酸弱碱盐,铵根离子水解导致溶液呈酸性,溶液的pH<7,故B错误;
C.Na2CO3是强碱弱酸盐,碳酸根离子水解导致溶液呈碱性,溶液的pH>7,故C正确;
D.Cu(NO3)2是强酸弱碱盐,铜离子水解导致溶液呈酸性,溶液的pH<7,故D错误;
故选C.
点评 本题以溶液酸碱性判断为载体考查盐类水解,明确盐的类型与溶液酸碱性关系即可解答,熟悉常见盐的类型,注意:温度未知时不能根据溶液pH判断酸碱性,为易错点.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
2.下列关于炔烃的描述中,不正确的是( )
| A. | 分子里含有-C≡C-的不饱和链烃 | |
| B. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色,但原理不同 | |
| C. | 分子里所有的碳原子都在一条直线上 | |
| D. | 碳原子数相同的炔烃和二烯烃是同分异构体 |
3.下列有关化学用语表示正确的是( )
| A. | 中子数为20的氯原子:${\;}_{17}^{37}$Cl | B. | H2O2的电子式: | ||
| C. | 硫原子的结构示意图: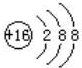 | D. | 甲烷分子的比例模型: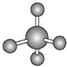 |
20.可以用分液漏斗分离的一组液体混合物是( )
| A. | 碘和四氯化碳 | B. | 苯和溴苯 | C. | 甘油和水 | D. | 汽油和水 |
7.在人类已知的化合物中,种类最多的是( )
| A. | 过渡元素形成的化合物 | B. | ⅢA族元素形成的化合物 | ||
| C. | ⅣA族元素形成的化合物 | D. | ⅦA族元素形成的化合物 |
17.下列物质中所有原子都有可能在同一平面上的是( )
| A. | 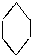 | B. | 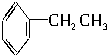 | C. | 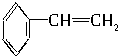 | D. | 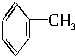 |
4.雷雨天闪电时空气中有臭氧(O3)生成,下列说法正确的是( )
| A. | O2和O3互为同位素 | |
| B. | O2和O3的相互转化是化学变化 | |
| C. | O3是由3个氧原子构成的化合物 | |
| D. | 等物质的量O2和O3含有相同的质子数 |
1.用括号内的物质除去试剂中少量的杂质,正确的是( )
| A. | 乙烷中的乙烯(氢气) | B. | 乙酸乙酯中的乙酸(饱和Na2CO3) | ||
| C. | 溴苯中的溴(苯) | D. | 乙烯中的SO2(KMnO4溶液) |
2.下列反应中,属于取代反应的是( )
| A. | CH4+2O2$\stackrel{点燃}{→}$ CO2+2H2O | B. | CH2=CH2+H2 $\stackrel{催化剂}{→}$ CH3-CH3 | ||
| C. |  | D. |  |