题目内容
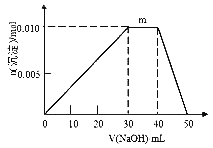
【题目】向盛有10mLlmol/LNH4Al(SO4)2溶液的烧杯中滴加1mol/LNaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下。下列有关说法正确的是
A. 当加入50mLNaOH时,溶液中的溶质为NaAlO2
B. m点反应的离子方程式:NH4++OH-=NH3·H2O
C. NH4Al(SO4)2溶液中离子浓度由大到小的顺序是:c(SO42-)>c(Al3+)>c(NH4+)>c(H+)>c(OH-)
D. 若向NH4Al(SO4)2溶液改加20mL1.2mol/LBa(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为0.02mol
【答案】B
【解析】A.当加入50mLNaOH时,Al(OH)3完全溶解,溶液中的溶质为Na2SO4、NH3H2O及NaAlO2,故A错误;B.m点NH4+与氢氧根离子反应生成NH3H2O,其反应的离子方程式为NH4++OH-=NH3H2O,故B正确;C. NH4Al(SO4)2溶液中存在NH4+和Al3+的水解,溶液显酸性,则溶液中离子浓度由大到小的顺序是:c(NH4+)>c(SO42-)>c(Al3+)>c(H+)>c(OH-),故C错误;D.10mL 1molL-1 NH4Al(SO4)2溶液中Al3+ 物质的量为0.01mol,NH4+的物质的量为0.01mol,SO42-的物质的量为0.02mol,20mL 1.2 molL-1Ba(OH)2溶液中Ba2+物质的量为0.024mol,OH-为0.048mol,由SO42-+Ba2+=BaSO4↓,可知SO42-不足,故可以得到0.02mol BaSO4,
Al3++3OH-=Al(OH)3↓
0.01mol 0.03mol 0.01mol
反应剩余OH-为0.048mol-0.03mol=0.018mol,
NH4++OH-=NH3H2O
0.01mol 0.01mol
反应剩余OH-为0.018mol-0.01mol=0.008mol,
Al(OH)3+OH-=AlO2-+2H2O
0.008mol 0.008mol
故得到Al(OH)3沉淀为0.01mol-0.008mol=0.002mol,则最终得到固体为0.02mol+0.002mol=0.022mol,故D错误;答案为B。

 阅读快车系列答案
阅读快车系列答案