题目内容
9.已知弱酸的电离平衡常数如下表,下列选项正确的是( )| 弱酸 | H2CO3 | 水杨酸(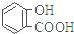 ) ) |
| 电离平衡常数(25℃) | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=1.3×10-3 Ka2=1.1×10-13 |
| A. | 常温下,等浓度、等体积的NaHCO3 溶液pH小于 溶液pH 溶液pH | |
| B. | 常温下,等浓度、等体积的Na2 CO3 溶液和 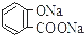 溶液中所含离子总数前者小于后者 溶液中所含离子总数前者小于后者 | |
| C. | 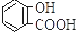 +2NaHCO3→ +2NaHCO3→ +2H2O+2CO2↑ +2H2O+2CO2↑ | |
| D. | 水杨酸的第二级电离 Ka2 远小于第一级电离Ka1 的原因之一是 能形成分子内氢键 |
分析 依据电离平衡常数比较形成盐的水解程度判断溶液酸碱性;酸性:水杨酸羧基酸性>H2CO3>HCO3->酚氧基,酸越弱形成盐的水解程度越大,
A.酸越弱,对应的酸根离子越容易水解,羧基水解程度小于碳酸氢根离子,据此判断两溶液的pH大小;
B.碳酸根离子水解程度大于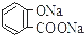 的水解程度,且碳酸根离子为二元弱酸根离子,而
的水解程度,且碳酸根离子为二元弱酸根离子,而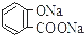 的酸根离子都是一元的,据此判断溶液中离子总数大小;
的酸根离子都是一元的,据此判断溶液中离子总数大小;
C.酚羟基的酸性小于碳酸,酚羟基不与碳酸氢根离子反应;
D. 中形成分子内氢键,使其更难电离出H+.
中形成分子内氢键,使其更难电离出H+.
解答 解:A.羧基水解程度小于碳酸氢根离子,常温下,等浓度、等体积的NaHCO3溶液pH大于 溶液pH,故A错误;
溶液pH,故A错误;
B.碳酸根离子水解程度大于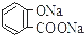 的水解程度,且碳酸根离子为二元弱酸根离子,而
的水解程度,且碳酸根离子为二元弱酸根离子,而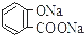 的酸根离子都是一元的,故等浓度、等体积的Na2CO3溶液和
的酸根离子都是一元的,故等浓度、等体积的Na2CO3溶液和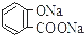 溶液中所含离子总数前者大于后者,故B错误;
溶液中所含离子总数前者大于后者,故B错误;
C.酚羟基的酸性小于碳酸,酚羟基不与碳酸氢根离子反应,只有羧基和碳酸氢钠溶液反应,故C错误;
D. 中形成分子内氢键,使其更难电离出H+,故相同温度下电离平衡常数Ka2<Ka1,故D正确;
中形成分子内氢键,使其更难电离出H+,故相同温度下电离平衡常数Ka2<Ka1,故D正确;
故选D.
点评 本题考查了弱电解质的电离、盐的水解原理及其影响等知识,题目难度中等,注意掌握弱电解质的电离平衡、盐的水解原理及其影响因素,试题充分考查了学生的分析、理解能力.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
19.短周期元素W、X、Y和Z的原子序数依次增大,其中W的阴离子的核外电子数与X,Y原子的核外内层电子数相同.X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用分离液态空气的方法来生产Y的单质,Z与X同族.下列说法中正确的是( )
| A. | 以上四种元素的原子半径大小为WXYZ | |
| B. | X的氢化物与水分子之间可形成氢键 | |
| C. | 已知Z-Cl键能比X-Cl键能小,所以Z的最简单氯化物比X的最简单氯化物沸点低 | |
| D. | W与Y可形成既含共价键又含离子键的化合物 |
17.某有机物X的结构简式为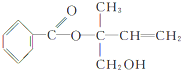 ,则下列有关说法正确的是( )
,则下列有关说法正确的是( )
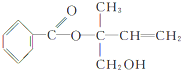 ,则下列有关说法正确的是( )
,则下列有关说法正确的是( )| A. | X的分子式为C12H16O3 | |
| B. | X在一定条件下能发生加成、加聚、取代、消去等反应 | |
| C. | 可用酸性高锰酸钾溶液区分苯和X | |
| D. | 在Ni作催化剂的条件下,1molX最多只能与1molH2加成 |
4.下列叙述中,正确的是( )
| A. | 在多电子的原子里,能量高的电子通常在离核近的区域内活动 | |
| B. | 核外电子总是先排在能量低的电子层上,例如只有排满了M层后才排N层 | |
| C. | 核外电子总是先排在能量低的电子层上 | |
| D. | 微粒的最外层只能是8个电子才稳定 |
14.X、Y、Z、W是浓度均为0.01mol/L的溶液,其溶质分别是HCl、NH4Cl、NaOH、NaF中的某一种.室温下,溶液的pH如下表:下列说法正确的是( )
| 溶液 | X | Y | Z | W |
| pH | 12 | 2 | 7.7 | 5.6 |
| A. | 将Z溶液加水稀释至浓度为0.001mol/L,所得溶液pH=6.7 | |
| B. | 四种溶液中,水的电离程度最大的是W溶液 | |
| C. | 将X、W溶液按1:2的体积比混合,所得溶液中:c(H+)>c(OH-) | |
| D. | 将11mLX溶液与9mLY溶液混合(忽略混合时体积的变化),所得溶液pH=10 |
1.下列选项中,离子方程式书写正确的是( )
| A. | 向Fe(NO3)2和KI混合溶液中加入少量稀盐酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ | |
| B. | 泡沫灭火器的灭火原理:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑ | |
| C. | 向硝酸银溶液中加入足量的氨水:Ag++2NH3•H2O=Ag(NH3)2++2H2O | |
| D. | 用足量的氨水处理硫酸工业的尾气:SO2+NH3•H2O=NH4++HSO3- |
18.用下列装置图进行相应的实验,其中正确的是( )
| A. | 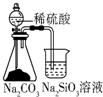 用如图可比较硫、碳、硅三种元素的非金属性强弱 | |
| B. | 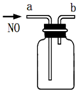 用如图装置收集一瓶纯净的NO | |
| C. |  用如图装置中U型管两端有液面差且保持不变时证明装置不漏气 | |
| D. | 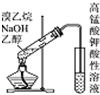 用如图检验溴乙烷与NaOH的醇溶液共热产生的乙烯 |
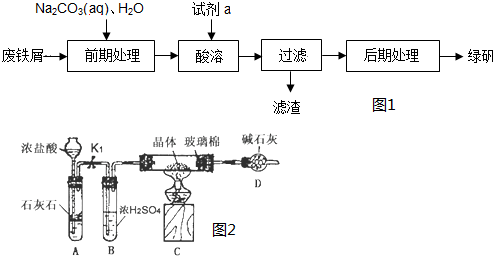
 SiCl4在室温下为无色液体,易挥发,有强烈的刺激性.把SiCl4先转化为SiHCl3,再经氢气还原生成高纯硅.
SiCl4在室温下为无色液体,易挥发,有强烈的刺激性.把SiCl4先转化为SiHCl3,再经氢气还原生成高纯硅.