��Ŀ����
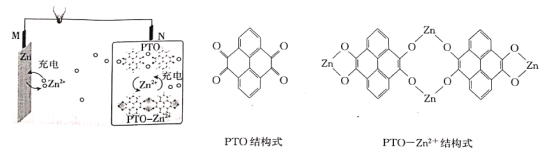
����Ŀ��298 Kʱ����20.0 mL 0.10 mol��L��1��ˮ�е���0.10 mol��L��1�����ᣬ��Һ��pH����������������ϵ��ͼ��ʾ����֪0.10 mol��L��1��ˮ�ĵ����Ϊ1.32%�������й�������ȷ����

A.�õζ�����Ӧ��ѡ���̪��Ϊָʾ��
B.M���Ӧ���������Ϊ20.0 mL
C.M�㴦����Һ��c(NH4+)��c(Cl��)��c(OH��)
D.N�㴦����Һ��pH��12
���𰸡�D
��������
A. ǿ������ζ�ʱ����������ǿ�������Σ�ʹ��Һ�����ԣ����ѡ�������ָʾ����
B. ���M����������Ϊ20.00mL����ô����ǡ����ȫ��Ӧ�����Ȼ�泥���ҺӦ�����ԣ�
C. M�㴦pH=7����Һ�����ԣ���c(H+)=c(OH-)�����ݵ���غ�ɵ�c(NH4+)��c(Cl��)���õ�ʱ��Һ������Ϊ�Ȼ�狀�NH3H2O��NH4+ˮ��ٽ�ˮ�ĵ��룬NH3H2O����ˮ�ĵ��룬NH4+ˮ���NH3H2O��������ƣ�
D. N��Ϊ��ˮ��Ũ��Ϊ0.1mol/L����ˮ�ĵ����Ϊ1.32%����ô��Һ��c(OH-)=0.10mol/L��1.32%=1.32��10-3mol/L������ˮ�����ӻ��ɼ����c(H+)����һ���ɼ����pH��
A. ǿ������ζ�ʱ����������ǿ�������Σ�ʹ��Һ�����ԣ�ʯ��ı�ɫ��pH��ΧΪ5-8�����ܺܺõĿ��Ƶζ��յ㣬���ѡ�������ָʾ����A�����
B. ���M����������Ϊ20.00mL����ô����ǡ����ȫ��Ӧ�����Ȼ�泥���ҺӦ�����ԣ���M��Ϊ���ԣ�����Ŀ�������B�����
C. M�㴦pH=7����Һ�����ԣ���c(H+)=c(OH-)�����ݵ���غ�ɵ�c(NH4+)��c(Cl��)���õ�ʱ��Һ������Ϊ�Ȼ�狀�NH3H2O��NH4+ˮ��ٽ�ˮ�ĵ��룬NH3H2O����ˮ�ĵ��룬NH4+ˮ���NH3H2O��������ƣ�ˮ�ĵ���̶Ⱥ�С�������Һ�и����ӵ�Ũ�ȴ�С˳��Ϊ��c(NH4+)��c(Cl��)> c(H+)=c(OH-)��C�����
D. N��Ϊ��ˮ��Ũ��Ϊ0.1mol/L����ˮ�ĵ����Ϊ1.32%����ô��Һ��c(OH-)=0.10mol/L��1.32%=1.32��10-3mol/L������ˮ�����ӻ��ɵ�c(H+)=![]() =7.6��10-12mol/L�� �����Һ��pH<12��D����ȷ��
=7.6��10-12mol/L�� �����Һ��pH<12��D����ȷ��
��ѡD��

 ���������������Բ��������ϵ�д�
���������������Բ��������ϵ�д�����Ŀ����H2O2��KI��ϴ�ྫ����ɡ��������ࡱʵ�飨��ʱ���ڲ���������ĭ����ijͬѧ�����������϶Ը�ʵ�����̽����
��1������1��KI�ڸ÷�Ӧ�е����ã�
H2O2��I����H2O��IO����H2O2��IO����H2O��O2����I�����ܷ�Ӧ�Ļ�ѧ����ʽ��________________��
��2������2��H2O2�ֽⷴӦ�����������仯��ͼ��ʾ�����Т���KI���룬����KI���롣�����ж���ȷ����___________������ĸ����
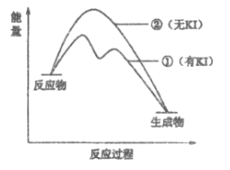
a. ����KI��ı��˷�Ӧ��·��
b. ����KI��ı����ܷ�Ӧ�������仯
c. H2O2��I����H2O��IO���Ƿ��ȷ�Ӧ
��3��ʵ���з��֣�H2O2��KI��Һ��Ϻ����������ݣ���Һ��ɫ��ơ��ټ���CCl4�������ã��������Լ��١�
����3��I2Ҳ�ɴ�H2O2�ķֽⷴӦ��
�ټ�CCl4�������úɹ۲쵽___________��˵����I2���ɡ�
���������Լ��ٵ�ԭ������ǣ�i. H2O2Ũ�Ƚ��ͣ�ii. ________�����¶���ʵ��˵��i������Ҫԭ����H2O2��Һ�м���KI��Һ������Һ��ƺֳ����ȷ���A��B���Թ��С�A�Թܼ���CCl4��B�Թܲ���CCl4���ֱ������á��۲쵽��������_____________��
��4������4��I����aq����I2��aq��![]() I3����aq�� K��640��
I3����aq�� K��640��
Ϊ��̽����ϵ�к������Ĵ�����ʽ������ʵ�飺��20 mLһ��Ũ�ȵ�H2O2��Һ�м���10mL 0.10mol��L��1 KI��Һ����ƽ��������Ũ�����£�
�� | I�� | I2 | I3�� |
Ũ��/��mol��L��1�� | 2.5��10��3 | a | 4.0��10��3 |
��a��__________��
�ڸ�ƽ����ϵ�г��˺���I����I2��I3���⣬һ��������������������������________________��
����Ŀ�������£���0.05 mol Na2CO3��������ˮ���100 mL��Һ������Һ�м����������ʣ��йؽ�����ȷ����(����)
�������� | ���� | |
A | 50 mL 1 mol��L��1H2SO4 | ��Ӧ������c(Na��)��c(SO |
B | 0.05 mol CaO | ��Һ�� |
C | 50 mL H2O | ��ˮ�������c(H��)��c(OH��)���� |
D | 0.1 mol NaHSO4���� | ��Ӧ��ȫ����ҺpH��С��c(Na��)���� |
A. A B. B C. C D. D
����Ŀ��Ǧ���������ұ������Ǧ������Ҫ�ɷ�ΪPbS��
I������Ǧ��Ǧ�����ڿ����б��գ�����PbO��SO2��
��1����Ǧ�������Ǧ�ķ�Ӧ�Ļ�ѧ����ʽΪ_________��
��2������Ǧ�ķ����к���Ũ��SO2���ɽ�����ͨ�������ˮ�н��д�������Ӧ�����ӷ���ʽΪ��____��
II��ʪ����Ǧ���Ʊ�����Ǧ��ͬʱ�������Ƶ���ǣ�����ڻ���Ǧ��Ϊ������ʪ����Ǧ�Ĺ����������£�

��֪���� ��ͬ�¶���PbCl2���ܽ�����±���ʾ��
�¶�/�� | 20 | 40 | 60 | 80 | 100 |
�ܽ��/g | 1.00 | 1.42 | 1.94 | 2.88 | 3.20 |
�� PbCl2Ϊ������ˮ��������ʣ���Cl��Ũ�Ƚϴ����Һ�У�����ƽ�⣺ PbCl2��aq��+2Cl����aq�� ![]() PbCl42����aq��
PbCl42����aq��
��3����ȡҺ��FeCl3��������_________��
��4�������Ϣ�жϣ�����aΪ_________��������PbCl2��������
��5������Һ3����Һ2�ֱ�������ͼ��ʾ���װ�õ����������У�����ȡ����Ǧ��ʹ��ȡҺ�е�FeCl3������
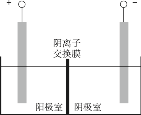
�� ��Һ3Ӧ����______�����������������������������С�
�� ������Һ2��������ΪFeCl3�Ŀ���ԭ����______��
�� ��Ǧ���������Ϊa g��Ǧ������Ϊb����������ͨ��c mol����ʱ������Ǧȫ��������Ǧ������PbS�����������ļ���ʽΪ______��